Потенциодинамическая кривая
Cтраница 1
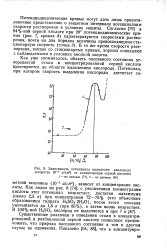 |
Зависимость потенциала выделения кислорода ( скорость 10 - 5 afcM2 от концентрации серной кислоты / - по данным, 2 - по данным. [1] |
Потенциодинамические кривые могут дать лишь ориенти ровочное представление о защитном интервале потенциалов и скорости растворения в условиях защиты. В то же время скорости растворения, взятые со стационарных кривых, хорошо совпадают с наблюдаемыми в условиях анодной защиты. [2]
Потенциодинамические кривые являются производными от кривых заряжения, с их помощью иногда удается более детально исследовать границу электрод - раствор. Но основное преимущество перед кривыми заряжения состоит в том, что периодическое окисление и восстановление электрода стабилизирует состояние его поверхности, уменьшается влияние загрязнений, поэтому Потенциодинамические кривые лучше воспроизводятся. [3]
 |
Гальваностатические кривые окисления гидразина на чернях ( / - 5 и. [4] |
Потенциодинамическая кривая, полученная при развертке потенциала из анодной области в катодную, как и на платине, идет выше кривой, регистрирующей при развертке потенциала из катодной области в анодную. Это обусловлено развитием поверхности электрода при восстановлении оксидов гидразином. [5]
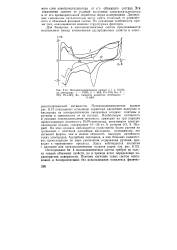 |
Потенциодинамические кривые в 1 н. H2SC4. [6] |
Потенциодинамические кривые рис. 8.13 показывают изменение характера адсорбции водорода и кислорода на электролитически смешанных осадках платины и рутения в зависимости от их состава. Наибольшую активность в реакции электроокисления метанола, примерно на три порядка превосходящую активность Pt / Pt-электрода, показывают электролитические осадки, содержащие 15 - 20 ат. На этих осадках наблюдается существенно более ранняя по сравнению с платиной адсорбция кислорода, по-видимому, его активной формы, чем и можно объяснить высокую активность таких электродов. Адсорбция кислорода, в еще больших количествах происходящая по мере увеличения содержания рутения, приводит к торможению процесса. Исследование би - и поликомпонентных систем требует не только знания объемных свойств, но и прежде всего определения характеристик поверхности. [7]
На рис. 7.13 изображена потенциодинамическая кривая на платиновом электроде в растворе серной кислоты. Два максимума 1 и 2 соответствуют двум формам адсорбированного водорода - так называемого прочно - и слабосвязанного водорода. Точное совпадение максимумов при прямой и обратной развертке напряжения свидетельствует об обратимости процесса адсорбции водорода. В средней части кривой значения тока низки и характеризуют двойнослойную область. Слабовыраженный пик 3 при положительных потенциалах связан с адсорбцией кислорода, ему соответствует катодный максимум восстановления 4, сильно смещенный в отрицательную сторону из-за необратимости процесса посадки - снятия кислорода. [8]
Последовательность операций при измерении потенциодинамических кривых сохраняется такой же и исходный потенциал выбирается на основе тех же принципов, что и при измерении кривых заряжения. Измерения проводят при 3 - 4 скоростях наложения потенциала в различных интервалах изменения потенциала. [9]
Методом кривых заряжения и потенциодинамических кривых исследованы свойства платино-титановых скелетных катализаторов с различным содержанием титана. На основании полученных данных рассчитан ряд характеристик исследованных катализаторов по отношению к процессу адсорбции водорода, сделан рентгенофазный анализ изученных образцов. Полученные результаты сопоставлены с каталитической активностью указанных электродов-катализаторов в реакции восстановления нитрометана и сделаны предположения относительно механизма этого процесса. [10]
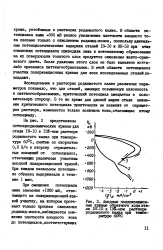 |
Анодные поляризационные кривые обратного хода стали 18 - Ю в 15 % - ном растворе роданистого калия при температуре 60 С. [11] |
На рис. 2 представлены у потенциодинамические кривые для нВ стали 18 - Ю в 15 / 6-ном растворе - 200 роданистого калия при температуре 60 С, снятые со скоростью 0 9 В / ч в сторону отрицательных значений от потенциалов, отвечающих различным участкам анодной поляризационной кривой. [12]
Исследованы кинетики электродных потенциалов и сняты потенциодинамические кривые при скорости изменения потенциала 0 5 В / мин. Наряду с покрытиями из меди и латуни испытаны медные и цинковые конденсаты. [13]
Циклические вольтамперограммы представляют собой полученные по трехэлектродной схеме потенциодинамические кривые с импульсной разверткой потенциала, как правило, имеющей форму равнобедренного треугольника. По этой причине циклическую вольтамперметрию иногда называют методом треугольного импульса потенциала. [14]
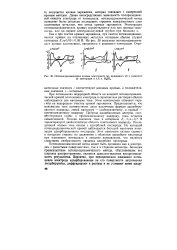 |
Потенциодинамические кривые платинового ( а, иридиевого ( б и родиевого ( в электродов в 4 6 н. HaS04. [15] |
Страницы: 1 2 3 4