Бальхаузен
Cтраница 2
Илзе и Хартмана [28], которые применили ее для объяснения слабой полосы поглощения в видимой части спектра иона гекса-аквотитана ( III), Вслед за ними Оргел [29], вероятно в большей мере, чем любой другой химик, развил эту теорию и указал на важное значение ее для изучения комплексов переходных металлов. В последнее десятилетие большой вклад в эту теорию и ее применение в химии комплексных соединений сделали Иор-генсек, Бальхаузен, Гриффите, Ньюхольм, Оуен, Коттон и многие другие. Эти же химики в основном последовательно развили и применили теорию поля лигандов, изложенную ниже. [16]
Первый из них был выполнен Шусторовичем и Дяткиной [94] с использованием слэтеровских атомных функций; во втором расчете, выполненном Далем и Бальхаузеном [95], для атома железа вместо слэтеровских были использованы функции Хартри - Фока, рассчитанные Уотсоном. [17]
Популярное объяснение эффекта Яна - Теллера см. в разд. Несложное математическое описание эффекта приведено в разд. Бальхаузена [49], полное и интересное обсуждение спектроскопических явлений, связанных с эффектом, дано в разд. Простые примеры даны на стр. [18]
Чтобы получить собственное значение волновой функции для - электронов путем решения волнового уравнения, необходимо использовать математический аппарат квантовой механики. Но это выходит за рамки книги. Интересующемуся читателю следует обратиться к книгам Бальхаузена [30] и Фиджиса [31], в которых можно найти математические детали теорий кристаллического поля и поля лигандов, а также к книге Гриффитса [32], в которой наиболее исчерпывающе изложен этот вопрос. [19]
Поправочный терм для d2 - и частично для tf - систем возникает вследствие конфигурационных взаимодействий, на которых мы не будем подробно останавливаться. Поправки для d - и сР - систем возникают как следствие дополнительного межэлектронного взаимодействия, имеющего место в этих системах. Математические выражения для энергетических уровней в слабых, сильных и в промежуточных кристаллических полях приведены в книге Бальхаузена [10] и здесь будут опущены. [21]
Следует, правда, иметь в виду, что изменения энергии электронного уровня, которые мы описываем с помощью параметров кристаллического поля, в действительности обусловлены и кристаллическим полем, и ковалентностью. Заметим, что обе точки зрения объединены в новейшей теории поля лигандов, в которой одновременно учитываются и ковалентность, и электростатические эффекты. Более подробно познакомиться с теорией молекулярных орбит и с современной теорией поля лигандов можно по книгам Оргеля [66], Бальхаузена [67] или по статье Мак-Клюра [68], а также по цитированной там литературе. [22]
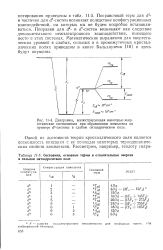
Количественные диаграммы уровней энергии для многоэлектронных конфигураций d в кубических полях могут быть получены на основе теории поля лигандов. Они являются необходимой базой для расшифровки спектров поглощения и оценки параметров Dq. Эти диаграммы охватывают все многоэлектронные конфигурации dn в октаэдрических полях. Более точные диаграммы, учитывающие спин-орбитальное взаимодействие, были построены Лиром [36] для конфигураций d1 и d9, Лиром и Бальхаузеном [37] для V ( III) конфигурации d2, и Ni ( II) конфигурации d8, в октаэдрических и тетраэдрических полях и Лиром [38] для Сг ( III) конфигурации d3, и Со ( II) конфигурации d7, также в октаэдрических и тетраэдрических полях. Используя эти диаграммы, следует помнить, что теоретические положения, на которых они основаны, приближенны и что поля лигандов не обязательно имеют кубическую симметрию. [23]
 |
Выбор системы координат для Октаэдри-ческого комплекса [ MLeJn. [24] |
Теория кристаллического поля дает мощный аппарат для качественного, а щюгда и количественного исследования свойств комплексных соединений. Однако один из ее существенных недостатков состоит в том, что она рассматривает лишь электрический характер влияния лигандов на центральный ион. Поэтому с помощью теории кристаллического поля можно решать только те вопросы, которые связаны с изменением электронной конфигурации металла под воздействием поля лигандов и нельзя касаться перераспределения электронной плотности при комплексообразовании, которое обусловливает прочность образующихся химических связей. Модифицированной теорией, приспособленной к рассмотрению ковалентных связей в координационных соединениях, явилась созданная в 50 - х годах Ор-гелом, Иоргенсеном и Бальхаузеном теория поля лигандов, объединившая в себе достижения теории кристаллического поля и метода молекулярных орбиталей. [25]
В настоящей книге химическая связь рассматривается главным образом с точки зрения теории молекулярных орбиталей. Там, где это представляется необходи -; мым, метод МО сравнивается с методом валентных связей и с теорией кристаллического поля. Книга рассчитана на студентов, не имеющих представления о теории групп. Хотя при изложении теории МО используются / принципы симметрии, формальные теоретико-групповые методы при этом не привлекаются, и только в главе IX применены символы теории групп. Профессором Карлом Бальхаузеном и автором опубликован конспект вводного курса по теории МО, написанный на несколько более высоком уровне, чем настоящая книга. В этом конспекте уделено большое внимание применению теории групп к вопросам электронного строения молекул. [26]
Теория кристаллического поля не нова. К комплексам переходных металлов эта теория впервые была применена Шлаппом и Пенни 19 и Ван - Флеком20, которые использовали ее для вычисления магнитной восприимчивости. В 1935 г. Ван - Флек21 обобщил и сравнил метод валентных связей, теорию кристаллического поля и метод молекулярных орбиталей. Однако в последующие двадцать лет теорией кристаллического поля пользовалось ограниченное число физиков для изучения главным образом тонких деталей магнетохимии и спектров поглощения. Вслед за ними Оргел23, вероятно в большей мере, чем любой другой химик, развил эту теорию и указал на важное значение ее для изучения комплексов. В последнее десятилетие большой вклад в эту теорию и ее применение в химии комплексных соединений сделали йоргенсен, Бальхаузен, Бьеррум, Гриффите, Ньюхольм, Оуен, Лир и многие другие. [27]
Хотя эта теория применима и к соединениям, в которых кристаллическое поле влияет на степень вырождения d - орбиталей, наибольшего успеха и самого широкого распространения она достигла в описании комплексов переходных металлов, в которых внешние электроны находятся на d - орбиталях. Теория кристаллического поля не нова. К комплексам переходных металлов эта теория впервые была применена Шлаппом и Пенни19 и Ван - Флеком20, которые использовали ее для вычисления магнитных восприимчивостей. В 1935 г. Ван - Флек21 обобщил и сравнил метод валентных связей, теорию кристаллического поля и метод молекулярных орбиталей. Однако в последующие двадцать лет теорией кристаллического поля пользовалось ограниченное число физиков, главным образом для изучения тонких деталей магнетохимии и спектров поглощения. Вслед за ними Оргел23, вероятно в большей мере, чем любой другой химик, развил теорию кристаллического поля и указал на ее важное значение для изучения комплексов. В последнее десятилетие большой вклад в эту теорию и ее применение в химии комплексных соединений сделали Йоргенсен, Бальхаузен, Бьеррум. Гриффите, Ньюхольм, Оуен, Лир и многие другие. Для свободных ионов или атомов в вакууме эти орбитали вырождены; при наложении электрического поля, обусловленного, например, наличием лигандов, энергии этих орбиталей дифференцируются. Энергии орбиталей, направленных к лигандам, повышаются по сравнению с энергией орбиталей, направленных между ними. Например, если шесть одинаковых лигандов приближаются к иону металла по осям х, у и z, заряды лигандов будут в большей степени отталкивать электрон, находящийся на dz2 - или d / 2-орбитали, чем на орби-талях dxy, dxz и dyz, так как первые направлены к лигандам. [28]
Хотя эта теория применима и к соединениям, в которых кристаллическое поле влияет на степень вырождения d - орбиталей, наибольшего успеха и самого широкого распространения она достигла в описании комплексов переходных металлов, в которых внешние электроны находятся на d - орбиталях. Теория кристаллического поля не нова. К комплексам переходных металлов эта теория впервые была применена Шлаппом и Пенни19 и Ван - Флеком20, которые использовали ее для вычисления магнитных восприимчивостей. В 1935 г. Ван - Флек21 обобщил и сравнил метод валентных связей, теорию кристаллического поля и метод молекулярных орбиталей. Однако в последующие двадцать лет теорией кристаллического поля пользовалось ограниченное число физиков, главным образом для изучения тонких деталей магнетохимии и спектров поглощения. Вслед за ними Оргел23, вероятно в большей мере, чем любой другой химик, развил теорию кристаллического поля и указал на ее важное значение для изучения комплексов. В последнее десятилетие большой вклад в эту теорию и ее применение в химии комплексных соединений сделали Йоргенсен, Бальхаузен, Бьеррум. Гриффите, Ньюхольм, Оуен, Лир и многие другие. Для свободных ионов или атомов в вакууме эти орбитали вырождены; при наложении электрического поля, обусловленного, например, наличием лигандов, энергии этих орбиталей дифференцируются. Энергии орбиталей, направленных к лигандам, повышаются по сравнению с энергией орбиталей, направленных между ними. Например, если шесть одинаковых лигандов приближаются к иону металла по осям х, у и z, заряды лигандов будут в большей степени отталкивать электрон, находящийся на dZ2 - или d - - орбитали, чем на орби-талях dxy, dxz и dyz, так как первые направлены к лигандам. [29]
Хотя эта теория применима и к соединениям, в которых кристаллическое поле влияет на степень вырождения d - орбиталей, наибольшего успеха и самого широкого распространения она достигла в описании комплексов переходных металлов, в которых внешние электроны находятся на d - орбиталях. Теория кристаллического поля не нова. К комплексам переходных металлов эта теория впервые была применена Шлаппом и Пенни19 и Ван - Флеком20, которые использовали ее для вычисления магнитных восприимчивостей. В 1935 г. Ван - Флек21 обобщил и сравнил метод валентных связей, теорию кристаллического поля и метод молекулярных орбиталей. Однако в последующие двадцать лет теорией кристаллического поля пользовалось ограниченное число физиков, главным образом для изучения тонких деталей магнетохимии и спектров поглощения. Илзе и Хартмана22, которые применили ее для объяснения слабой полосы поглощения в видимой части спектра иона гексааквотитана ( III) Вслед за ними Оргел23, вероятно в большей мере, чем любой другой химик, развил теорию кристаллического поля и указал на ее важное значение для изучения комплексов. В последнее десятилетие большой вклад в эту теорию и ее применение в химии комплексных соединений сделали Йоргенсен, Бальхаузен, Бьеррум. Гриффите, Ньюхольм, Оуен, Лир и многие другие. Для свободных ионов или атомов в вакууме эти орбитали вырождены; при наложении электрического поля, обусловленного, например, наличием лигандов, энергии этих орбиталей дифференцируются. Энергии орбиталей, направленных к лигандам, повышаются по сравнению с энергией орбиталей, направленных между ними. Например, если шесть одинаковых лигандов приближаются к иону металла по осям х, у и 2, заряды лигандов будут в большей степени отталкивать электрон, находящийся на d22 - или 2 иг-орбитали, чем на орби-талях dxy, dxz и dvz, так как первые направлены к лигандам. [30]
Страницы: 1 2