Надперекись
Cтраница 2
Супероксиды ( надперекиси) типа Э2О4 известны для калия, рубидия и цезия. [16]
Супероксид ( надперекись) калия К2О4 образуется при сгорании калия в избытке кислорода. [17]
Известна также малоустойчивая надперекись водорода Н2О4, существующая при низких температурах. [18]
Химические свойства надперекиси еще исследованы недостаточно подробно. Несомненно только, что вне зависимости от своего происхождения она является сильным окислителем. [19]
При синтезе надперекиси цезия вышеуказанным способом получаются две фракции. Эта фракция является наиболее чистой и представляет собою легкий, пушистый светло-желтый порошок. [20]
Под действием воды надперекись рубидия разлагается на гидроокись рубидия, перекись водорода и кислород. [21]
Кроме щелочных металлов надперекиси известны только для элементов подгруппы кальция. При хранении вне контакта с воздухом они устойчивы, а с водой бурно взаимодействуют, отщепляя надперекисный кислород. [22]
Окислы, перекиси или надперекиси образуются в зависимости от условий получения и от природы металла. [23]
Если в водных растворах надперекисей возникает равновесие, выражаемое уравнением 3, то можно прийти к той же реакции, если соединить вместе растворы гидроокисей и перекиси водорода при температурах, исключающих заметное разложение последней. [24]
Предпринятые нами попытки получения надперекиси цезия высокой чистоты при окислении больших навесок металла кислородом были неудачными, так как образовывалась монолитная масса промежуточных окисей, доокисление которых протекало с большим трудом и в течение длительного времени. [25]
Это подтверждается тем, что кристаллическая надперекись КО2 парамагнитна и обладает магнитной восприимчивостью, равной примерно 2 магнетонам Бора ( что соответствует одному неспаренному электрону; стр. Ион О - имел бы четное число электронов и, следовательно, был бы диамагнитным. [26]
Наиболее подходящим методом получения перекиси или надперекиси определенного металла является один из следующих трех: 1) нагревание металла или окиси его в кислороде или на воздухе; 2) окисление в жидком аммиаке; 3) реакция соединения металла с перекисью водорода, обычно в присутствии добавленной щелочи. [27]
В воде как перекиси, так и надперекиси щелочноземельных металлов растворяются с трудом. [28]
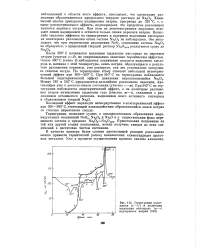 |
Термограмма разложения ( а. - к и политерма выделения кислорода ( а-к надперекиси натрия. [29] |
При этом на рентгенограммах порошков исчезают линии надперекиси и остаются только линии перекиси натрия. [30]
Страницы: 1 2 3 4