Надперекись - натрий
Cтраница 1
 |
Получение кислорода разложением перекиси водорода. [1] |
Надперекиси натрия и калия ( общая формула Ме02) представляют собой твердые кристаллические вещества ярко-желтого цвета. Они широко известны как эффективные средства регенерации воздуха в различных системах жизнеобеспечения. Их действие основано на чрезвычайно высокой активности к воде и водяному пару в широком интервале температур. [2]
Надперекись натрия Na02 образуется при действии кислорода на перекись натрия при повышенной температуре и давлении. Перекиси MgO2, CaO2 и ВаО2 могут быть получены при взаимодействии соответствующих гидроокисей с перекисью водорода или солей с Н2О2 в присутствии аммиака. [3]
 |
Получение кислорода гидролизом иадперекиси натрия. [4] |
Надперекиси натрия и калия устойчивы при хранении в герметичной таре и начинают разлагаться при температурах выше 100 СС. [5]
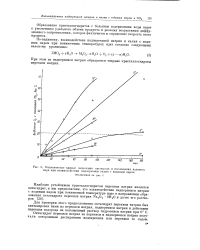 |
Кинетические кривые выделения кислорода и поглощения водяного пара при взаимодействии надперекиси калия о водяным паром. [6] |
При этом из надперекиси натрия образуются твердые кристаллогидраты перекиси натрия. [7]
Выход кислорода при гидролизе надперекиси натрия состав - Из резервуара 1 перекись насосом 2 подается в реактор 3, где происходит ее разложение; образовавшаяся парогазовая смесь направляется в холодильник-конденсатор 4, где происходит ее охлаждение и отделение кислорода от влаги. Очищенный кислород направляется в ЭХГ. Как видно, схема достаточно проста, однако некоторые свойства перекиси водорода резко снижают достоинства этого способа хранения кислорода. [8]
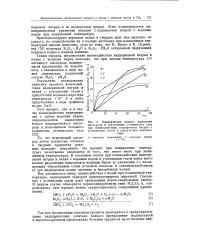 |
Кинетические кривые выделения кислорода и поглощения углекислого газа при взаимодействии надперекиси натрия с углекислым газом в присутствии водяного пара. [9] |
Этим подтверждается вышеприведенное уравнение реакции 2 надперекиси натрия с водяным паром при пониженной температуре. [10]
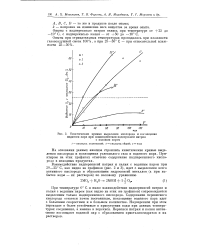 |
Кинетические кривые выделения кислорода и поглощения водяного пара при взаимодействии надперекисй натрия с водяным паром. [11] |
При температуре 0 С и ниже взаимодействие надперекисей натрия и калия с водяным паром ( как видно из этих же графиков) сопровождается выделением только надперекисного кислорода. Содержание перекисного кислорода остается почти постоянным, поглощение водяного пара идет с большими скоростями и в большом количестве. Надперекиои при этом переходят в более устойчивые в присутствии воды при данных температурах соединения, а именно в перекиси. Перекиси натрия и калия интенсивно поглощают водяной пар с образованием кристаллогидратов и их растворов. [12]
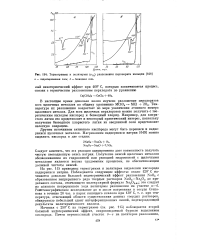 |
Термограммы и политермы ( у0г разложения перхлората кальция а - гидратированная соль. б - безводная соль. [13] |
На рис. 115 приведены термограмма и политерма выделения кислорода надперекиси натрия. Рентгенографическое исследование до и после нагревания в сосуде Степанова в течение 26 час. [14]
Полученные данные подтверждают выводы предыдущих ис следо-ваний [1-5] относительно характера взаимодействия надперекисей натрия и калия с водяным паром и углекислым газом. [15]
Страницы: 1 2 3