Анализ - кинетическая зависимость
Cтраница 1
Анализ кинетических зависимостей, описывающих гомогенные и гетерогенные каталитические процессы, показывает, что для равномерного превращения реагентов при максимальной производительности единицы катализаторного объема требуется определенная закономерность изменения температурного поля. [1]
 |
Графики за - Графически зависимость м / ( т висимости ш / ( т. дляну транения представлю. [2] |
Анализ кинетических зависимостей на рис. 2 - 6 показывает, что прямая 3 соответствует такой скорости протекания цепной реакции, при которой количество возникающих цепей равно числу обрыва цепей. Эти условия соответствуют температуре самовоспламенения. [3]
Анализ кинетических зависимостей выхода пиридиновых оснований от условного времени контакта при различных парциальных давлениях исходных компонентов ( I, II) показал, что реакция конденсации алифатических спиртов с формальдегидом и аммиаком ( реакции 5, 6), имеет первый порядок по спирту ( конверсия его и выход пиридиновых оснований в расчете на спирт не зависят от его парциального давления в пределах 0 012 - 0 02 МПа) ( рнс. [4]
Поэтому анализ кинетических зависимостей позволяет исключить одни варианты механизма и сделать предположения о наиболее вероятных вариантах. Рассмотрение кинетических уравнений позволяет также в некоторых случаях вынести суждение о правильности их интерпретации. [5]
Итак, анализ кинетических зависимостей, описывающих гомогенные и гетерогенные каталитические процессы, показывает, что для равномерного превращения реагентов при максимальной производительности единицы катализаторного объема требуется определенная закономерность изменения температурного поля. [6]
Таким образом, анализ кинетической зависимости позволил в данном случае сделать определенное предположение о механизме процесса, исключив десорбцию бензола как лимитирующую стадию. [7]
Изложенные ориентировочные рекомендации анализа кинетических зависимостей могут оказаться ненужными по мере развития использования электронно-вычислительной техники, когда соответствующие машины, соединенные с реакторами, будут в ходе опытов анализировать данные и выдавать кинетические уравнения и численные значения их постоянных. [8]
Вместе с опытами по непосредственному обнаружению метиленовых радикалов в зоне распада метана [173] приведенный выше анализ кинетических зависимостей, казалось, свидетельствует о большей вероятности механизма распада метана через метиленовые радикалы. Этот механизм казался более вероятным и в случае распада этана, поскольку, подобно СО, образование метилен-радикалов как более стабильных частиц может пройти энергетически более экономно. [9]
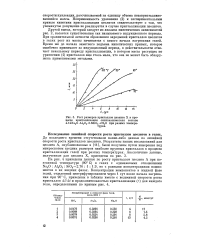 |
Рост размеров кристаллов цеолита X в процессе кристаллизации силикаалюмогеля состава NaaO - Al203 - SiOs. [10] |
Неприменимость уравнения ( 2) к экспериментальным кривым кинетики кристаллизации цеолитов свидетельствует о том, что упомянутое допущение не реализуется в случае кристаллизации цеолитов. Другой вывод, который следует из анализа кинетических зависимостей рис. 2, касается существования так называемого индукционного периода. При сравнительной легкости образования зародышей кристаллов цеолитов в гелях рост их массы начинается с самого начала нагревания гелей. Время же до начала заметного подъема кинетических кривых, которое ошибочно принимают за индукционный период, в действительности отвечает начальному периоду кристаллизации, в котором масса растущих по уравнению ( 4) кристаллов еще столь мала, что она не может быть обнаружена применяемыми методами. [11]
Поскольку представления о влиянии электронных факторов только начали развиваться, они ( кроме приведенных примеров) в большинстве случаев еще не доводятся до анализа конкретных кинетических зависимостей, а часто сводятся лишь к общим соображениям. [12]
Истинный характер кинетической зависимости, характеризуемой видом кинетического уравнения, может маскироваться условиями процесса. Так например, если реакция проводится в большом избытке концентрации одного из компонентов, то будет казаться, что скорость реакции от него не зависит. Аналогичным будет случай, когда концентрация данного компонента сохраняется постоянной в ходе реакции, например, вследствие поддержания постоянной упругости насыщенного пара этого вещества или постоянной его концентрации в растворе. Отсюда различают наблюдаемый, кажущийся и истинный порядки реакции. Поэтому при анализе кинетических зависимостей и составлении кинетических уравнений должны быть приняты во внимание все факторы, могущие влиять на их истинный характер. [13]
Страницы: 1