Анализ - биологический материал
Cтраница 2
Трудно переоценить значение метода в анализе биологических материалов, природных соединений, продуктов органического синтеза, фармацевтических препаратов, пищевых продуктов, в клиническом анализе, анализе минерального сырья и многих других материалов. [16]
 |
Прибор для отделения фторидов методом пирогидролиза. [17] |
Отделение фосфата чрезвычайно важно при анализе биологических материалов. Отделение фторида от анионов может осложниться присутствием фторидных комплексных ионов, таких, например, как ZrFe, AlFe, SiFe и др., которые не будут элюироваться вместе с фторидом, не связанным в комплекс. Описано [54] отделение фторида ( 25 мкг) от фосфата ( 12 5 мг Р) на смоле Дауэкс 1 с использованием 0 5 М раствора NaOH в качестве элюента. [18]
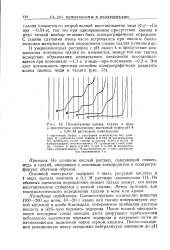 |
Подпрограмма свинца, таллия и меди. [19] |
Си - - Си при - 0 54 в), так что при одновременном присутствии свинца и меди таллий вообще не может быть полярографически определен. С такими случаями очень часто встречаются при анализе биологических материалов, при определении следов таллия всвинцеи др. В умереннокислых растворах с рН около 4 в присутствии ком-плексона потенциал таллия не изменяется, между тем как свинец вследствие образования комплексного соединения восстанавливается при потенциале - 1 1 в, а медь-при потенциале-0 3 в. [20]
Количественные и полуколичественные спектральные методы широко используются в анализе природных, технических и биологических материалов, а также при определении примесей в металлическом бериллии и его соединениях ( см. стр. [21]
Количественные и полуколичественные спектральные методы широко используются в анализе природных, технических и биологических материалов, а также при определении примесей в металлическом бериллии и его соединениях ( см. стр. [22]
Не менее четкие хроматограммы на бумаге получаются при использовании этанола в качестве основного растворителя. В этом случае получаются четкие хроматограммы; метод может быть использован для анализа биологических материалов. [23]
В последнем случае анализируемые породы предварительно сплавляют с карбонатом натрия, плав растворяют в НС1, добавляют как элемент внутреннего стандарта индий, раствор концентрируют и подвергают анализу. Используются линии Sr 4077 7 А и 4215 5 A, In - 4101 8 А. Возбуждение искрой используют в анализе биологического материала ( 156, 162) и радиоактивных веществ [163], а также других объектов. [24]
 |
Результаты определения сульфатов ( в % в пробах ( навеска - 1 г. [25] |
Колориметрический метод определения аммонийного азота с помощью реактива Несслера имеет высокую чувствительность, прост и удобен. Однако во многих случаях применение реактива Несслера для количественного определения иона аммония дает менее точные результаты, чем метод отгонки по Кьельдалю. В частности, это относится к анализу биологических материалов. При повышенном содержании в исследуемом растворе Mg, Ca, Fe и ряда других ионов образовавшийся при взаимодействии с аммиаком цветной коллоидный комплекс становится неустойчивым. Мешающие ионы вызывают его коагуляцию, вследствие чего происходит помутнение раствора, изменяется его оптическая плотность. [26]
При описании практического применения комплексометрии я стремился, чтобы глава эта не производила впечатления собрания одной только рецептуры, в которой приводятся отдельные прописи методов, не связанные между собой. Поэтому они даны здесь соответственно значению и вниманию, которое им уделено при разработке. В отдельных параграфах приводятся различные методы определения кальция и магния в разнообразных материалах, начиная с анализа воды и кончая анализами биологических материалов. [27]
Большинство лекарственных веществ поглощает в УФ-обла-сти спектра, что позволяет использовать для обнаружения УФ-детекторы. Чаще всего анализ ведут при 254 нм, несмотря на тот факт, что иногда удобнее работать при другой длине волны. С другой стороны, при этом возрастает как чувствительность анализа, так и селективность обнаружения, что весьма важно при анализе биологического материала. Известны также примеры использования дифференциальных рефрактометров, электрохимических детекторов, методов кулонометрии и масс-спектрометрии. [28]
При этом селен и теллур восстанавливаются до степени окисления 4 и отгоняются в виде галогенидов или оксогалогенидов. Концентрация кислоты должна быть выше 6 М, а температура выше 100 С. При дистилляции применяют смеси кислот, например НС1 - H2SO4, HBr - H2SO4, НСЮ4 - НВг. При анализе биологических материалов часто используют смесь Вг2 - НВг, причем Вг2 окисляет селен до Seiv. Избыток Вг2 отгоняется при более низкой температуре, чем селен. В присутствии НВг Sevi восстанавливается до Seiv. Отгоняющийся при дистилляции тетрабромид селена поглощают водой. [29]
Чтобы исключить внесение загрязнений из материала деталей пресса, поверхность стержней обрабатывают алмазным резцом. Стержни длиной около 10 мм используют в качестве электродов. Гомогенизация исследуемой пробы перед изготовлением электродов должна быть предельно высокой, потому что в про-пессе эксперимента расходуется небольшое количество вещества. Высокая воспроизводимость результатов ( 5 %) была достигнута в результате трехкратного растирания и последующего переплавления образца в платиновой капсуле. Эванс и Моррисон [91,92] при анализе озоленного биологического материала смешивали равные количества пробы и высокочистого графита. Гомогенизация образцов производилась в капсулах из карбида вольфрама в течение 30 мин. Смесь 1: 1 была выбрана с таким расчетом, чтобы вносить как можно меньше графита в пробу и, насколько возможно, уменьшить эффект, обусловленный различием концентраций элементов основы от образца к образцу. Эксперименты показали, что смесь, состоящая из равных количеств графита и золы, оптимальна. [30]
Страницы: 1 2 3