Анализ - межатомное расстояние
Cтраница 1
 |
Кремнекислородныи радикал [ Sie016 ] 6 -. [1] |
Анализ межатомных расстояний показывает, что и в случае германатов редкоземельных элементов порядки связей в гер-маниевокислородных радикалах определяются степенью их взаимодействия с катионами. [2]
Анализ межатомных расстояний в соединениях с М - донор-ными лигандами не дает вполне четкой картины взаимного влияния лигандов. Можно отметить лишь следующее. [3]
Анализ межатомных расстояний и валентных углов в координационном полиэдре не обнаруживает особых пространственных напряжений в лиганде при хелатообразовании, как это предполагалось в [45] для метионина. Примеры выполнения глицилглицином бидентатной функции приведены выше ( стр. [4]
Анализ межатомных расстояний показывает, что связь между атомами в соединении Mn4Si7 носит смешанный ковалентно-металличес-кий характер. Расстояния между атомами марганца в структуре превышают сумму атомных радиусов, поэтому взаимодействием этих атомов можно пренебречь. [5]
Следует отметить, что анализ межатомных расстояний в структурах оксиортосиликатов приводит к установлению определенной зависимости между длиной связи Si-О в кремне-кислородном тетраэдре и степенью взаимодействия концевого кислорода этой связи с катионами. Кроме того, установлена с небольшими отклонениями зависимость между средними расстояниями катион-кислород и кислород-кремний, выражающаяся в том, что укорочению расстояния катион-кислород соответствует удлинение связи О-Si, и наоборот. Все эти факты могут быть объяснены увеличением поляризации связи Si-О при уменьшении расстояния кислород-катион или при повышении координации по катионам концевого кислорода. [6]
Форма пирогруппы меняется, по-видимому, так, чтобы обеспечить соответствующее координационное число катиона. Анализ межатомных расстояний в исследованных соединениях позволяет заключить, что простая ( р - d) тг-теория [7] не дает удовлетворительного объяснения наблюдаемым закономерным изменениям длин связей в кремнекислородных анионах. Показано, что межатомные расстояния в пирогруппах определяются главным образом геометрией их расположения относительно катионов, обусловливающей величину поляризации связей. [7]
 |
Кристаллическая решетка a - ThSi2, по Брауэру и Митиусу ( 1942 г.. [8] |
Поскольку расстояния между атомами кремния в цепи и между цепями одинаковы, получается трехмерный каркас из этих атомов, в гнездах которого расположены атомы тория. Из анализа межатомных расстояний следует, что ThSi2 обладает структурой, промежуточной между дисилицидами переходных металлов и CoSi2 в котором преобладают неполярные связи. [9]
 |
Фталоцианид Pt. Проекция ас ряда электронной плотности. [10] |
Структура определена по проекции ас ряда электронной плотности ( рис. 414); координаты у найдены из геометрических соображений. Точность не выше 0 05 А, поэтому к анализу межатомных расстояний, следует отнестись критически. [11]
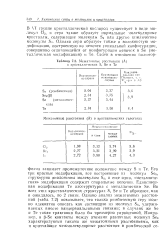 |
Межатомные расстояния ( А в кристаллических S, Se it Те. [12] |
Его три красные модификации, все построенные из молекул Se8, структурно аналогичны молекулам S8, и еще одна, металлическая модификация содержит спиральные цепочки. Единственная модификация Те изоструктурна с металлическим Se. Во всех этих кристаллических структурах S, Se и Те образуют, как и ожидалось, по 2 связи. Однако анализ межатомных расстояний ( табл. 7.2) показывает, что только ромбическую серу можно адекватно описать как состоящую из молекул Se, удерживаемых вместе вандерваальсовыми связями; в случаях же Se и Те такая трактовка была бы чрезмерно упрощенной. [13]
Можно перечислить ряд работ [11, 38, 93, 103], в которых г-фазы рассматриваются как электронные соединения. Блум и Грант [11] предположили, что составы о - фаз определяются электронной концентрацией, равной 210 электронам на элементарную ячейку или в среднем семи электронам на атом, а Гринфильд и Бек показали, что для среднего состава известных 0-фаз концентрация составляет 6 93 электрона на атом. По данным Бергмана и Шумейкера [7], вторая зона Бриллюэна может вместить 6 97 электрона на атом, что согласуется с приведенными выше данными. Это значение получено на основе анализа межатомных расстояний. [14]
Можно перечислить ряд работ [11, 38, 93, 103], в которых 0-фазы рассматриваются как электронные соединения. Блум а Грант [11] предположили, что составы ст-фаз определяются электронной концентрацией, равной 210 электронам на элементарную ячейку или в среднем семи электронам на атом, а Гринфильд и Бек показали, что для среднего состава известных о-фаз концентрация составляет 6 93 электрона на атом. По данным Бергмана и Шумепкера [7], вторая зона Бриллюэна может вместить 6 97 электрона на атом, что согласуется с приведенными выше данными. Это значение получено на основе анализа межатомных расстояний. [15]
Страницы: 1