Анализ - условие - равновесие
Cтраница 1
Анализ условий равновесия этих реакций показывает, что при - 700 С равновесный состав конечного газа определяется в основном реакциями ( III. Это следует из значений констант равновесия реакций ( III. [1]
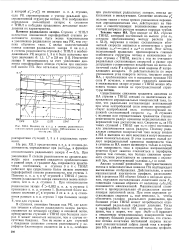 |
Влияние на к. п. д. и степень реактивности. [2] |
Анализ условий равновесия пространственного потока в межлопаточных каналах НА подтверждает высказанные соображения. Действительно, в месте максимальной изогнутости профиля, расположенной в решетках НА обычно ближе к входным кромкам, окружная составляющая лопаточной силы Fu, зависящая главным образом от величины czdcu / dz, оказывается максимальной. Максимальной становится и пропорциональная ей радиальная составляющая лопаточной силы. При этом окружная составляющая скорости си еще невелика, и, чтобы обеспечить условия радиального равновесия, при больших углах ТННЛ может потребоваться отрицательный радиальный градиент давления. [3]
Из анализа условий равновесия моста можно найти, что существуют минимальные значения г и гг, при которых возможен баланс. [4]
Для анализа условий равновесия равно-напряженной оболочки произвольной формы, нагруженной равномерным давлением и краевыми силами, применен принцип возможных перемещений. [5]
При анализе условий равновесия в статически неопределимых случаях для того, чтобы определить нормальные реакции NJ, приходится прибегать к гипотезе об упругости основания, либо к другим механическим моделям. [6]
Мощным методом анализа условий равновесия и устойчивости жидких тел является исследование возмущений. Будет показано, что равновесные состояния могут быть найдены из вариационного принципа: в равновесии энергия достигает экстремума. Частоты колебаний вблизи равновесного состояния могут быть найдены из рассмотрения малых отклонений от равновесия. Ниже мы разработаем формализм, необходимый для доказательства и использования этих принципов. [7]
Рассмотрим задачу анализа условий равновесия объекта в схвате на примере. [8]
Осуществленный Вальрасом, Джевонсом, Парето анализ условий равновесия рыночной экономики оказал большое влияние на бурж. Они упрощают, а часто и искажают реальные условия функционирования каниталистич. Достаточно указать па статичность этих моделей, на игнорировании противоречий п диспропорций, присущих капиталистич. [9]
Важную роль играют свойства потенциалов при анализе условий равновесия термодинамических систем. [10]
В качестве иллюстрации применения уравнений (6.43) - (6.48) для анализа условий равновесия в двухкомпонентных двухфазных системах мы рассмотрим равновесие жидкий раствор-пар. [11]
Дальнейшая детализация условий равновесия для конкретной сложной термодинамической системы может быть получена на основе анализа условий равновесия ( 156) совместно с условиями перераспределения вещества при фазовых переходах. Пусть, например, гетерогенная система состоит из ф фаз и п компонентов, так что в каждой фазе находятся все п компонентов. [12]
Жидкость помещают в резервуар, представляющий собой трехгранную пирамиду из пластин исследуемого вещества. Анализ условий равновесия позволяет написать систему уравнений, решение которых дает искомую величину YT - К сожалению, практического применения этот остроумный метод, очевидно, не нашел. [13]
Маловероятно, чтобы в ряду реакций с участием родственных соединений значения AS изменялись в широких пределах. Поэтому при анализе условий равновесия на всех стадиях процесса достаточно учитывать лишь значения ДЯ. Что касается скоростей, то, поскольку переходные состояния всех рассматриваемых стадий носят почти одинаковый характер, можно ожидать, что значения предэкспонента будут также приблизительно одинаковы. Как видно из предыдущего, различия в значениях АЯ определяются в основном различиями в изменении энергии л-электронов в ходе реакции. Отсюда следует вывод о том, что реакция, сопровождающаяся наименьшей убылью энергии л-электронов, должна протекать быстрее ( особенно на начальных стадиях, когда еще мало сказывается обратная реакция), а равновесие ее в большей степени сдвинуто в сторону образования конечных продуктов, чем в случае реакции, в ходе которой энергия я-электронов значительно убывает. [14]
При использовании в качестве термических переменных температуры и давления характеристической функцией для системы является изобарный потенциал. Поскольку при анализе условий равновесия между жидкой и паровой фазами смесей в качестве независимых переменных наиболее удобно принимать давление Р, температуру Т и составы фаз, для характеристики состояния системы обычно используют изобарный потенциал. [15]
Страницы: 1 2