Кислотные остатки
Cтраница 2
Кислотные остатки ( Cl1, N0s - и др.) для различных кислот различны, но общим для всех кислот будет наличие в растворах иона водорода. Отсюда следует, что общие свойства кислот ( кислый вкус, действие на лакмус, взаимодействие со щелочами, взаимодействие с металлами с выделением водорода и др.) определяются именно ионом водорода. [16]
Кислотные остатки могут содержать самые разные атомы. Основное требование, предъявляемое к их строению, чтобы связь между атомами в кислотных остатках была значительно прочнее связи между кислотным остатком и атомом водорода. Тем самым в химических превращениях обеспечивается высокая подвижность атомов водорода, которая придает кислотам ряд общих свойств. Напомним, что атом водорода в кислотах, как и в других соединениях, всегда одновалентен. [17]
Кислотные остатки обладают определенной основностью, которая определяется числом свободных валентностей у атомов кислорода. [18]
Кислотные остатки, идущие на солеобразование, подчеркнуты. [19]
Кислотные остатки представляют собой отрицательно-валентные группы атомов, не способные существовать как отдельное вещество. Отрицательная валентность кислотного остатка равна числу атомов водорода, удаленному из молекулы кислоты при образовании соли. Эту закономерность легко проследить по данным табл. 2 ( стр. [20]
Кислотные остатки у соединений четырехвалентной платины связаны с платиной очень прочно, и поэтому их вытеснение осуществляется с трудом; при действии аммиака на хлороплатина-ты получается смесь аммиакатов, и только в результате длительного воздействия аммиака можно получить пентаммины платины. Получение гексамминов платины сопряжено с очень большими трудностями. [21]
Кислотные остатки в ацидосоединениях двухвалентной платины замещаются аммиаком и аминами сравнительно легко. [22]
Кислотные остатки ( анионы) остаются в растворе. [23]
Кислотные остатки Ас входят в состав кислот и в состав солей. Валентность кислотного остатка определяется числом атомов водорода ( х) в молекуле кислоты. [24]
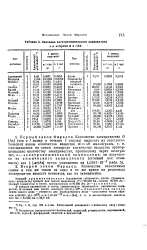 |
Значения электрохимического эквивалента ot в лег / кулон и в. / Ah. [25] |
Кислотные остатки кислот бромистой, йодистой, углекислоты, марганцевой, вотнсй, серией, фосфорной, соляной и хромистой. [26]
Кислотные остатки кислородных кислот, как, например: СО - SO, NOj, PO -, BrO, ClOj и др., являются также комплексными ионами. Правильно было бы эти кислотные остатки при написании заключать также в квадратные скобки, но этого обычно не делают. [27]
Кислотные остатки три-глицеридов жирных кислот молочного жира образуют с гидроксилами силикагеля водородные связи и удерживаются сорбентом. Согласно положениям М. А. Клисенко ( 1969), основанным на теории А. В. Киселева о специфическом и неспецифическом взаимодействии молекул с поверхностью адсорбента ( А. В. Киселев, Я. Н. Яшин, 1967), распределение пестицидов на колонке с силикаге-лем зависит от их химической структуры, свойств адсорбента и элюента. [28]
Такие кислотные остатки, как 80, N0, СН3СОСГ, сохраняют свои обычные названия, но чтобы отличить подобную группу от просто координированного кислотного остатка, к ее названию прибавляется буква ( А. [29]
 |
Пример хелатного комплекса. [30] |
Страницы: 1 2 3 4