Подгруппа - скандий
Cтраница 3
Чем отличаются атомы элементов подгруппы скандия от атомов элементов главной подгруппы III группы по строению электронных оболочек. Как это сказывается на их свойствах. [31]
В свободном состоянии элементы подгруппы скандия представляют собой серебристо-белые металлы с высокими температурами плавления. Металлические свойства выражены у них резче, чем у элементов главной подгруппы. Они растворяются в разбавленных соляной, азотной и серной кислотах, а при нагревании реагируют с большинством неметаллов. [32]
В свободном состоянии элементы подгруппы Скандия представляют собой серебристо-белые металлы с высокими температурами плавления. Металлические свойства выражены у них резче, чем у элементов главной подгруппы. Они растворяются в разбавленных соляной, азотной и серной кислотах, а при нагревании реагируют с большинством неметаллов. [33]
В земной коре элементы подгруппы скандия очень распылены и отдельных минералов не образуют. Из-за этого их трудно выделить в чилом ( без примесей) состоянии. [34]
В земной коре элементы подгруппы скандия очень распылены, отдельных минералов не образуют. Из-за этого их трудно выделить в чистом ( без примесей) состоянии. [35]
В земной коре элементы подгруппы скандия очень распылены и отдельных минералов не образуют. Из-за этого их трудно выделить в чистом ( без примесей) состоянии. [36]
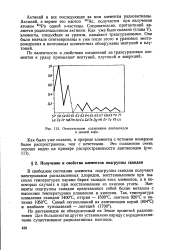 |
Относительное содержание лантаноидов в земной коре. [37] |
В свободном состоянии элементы подгруппы скандия получают электролизом расплавленных хлоридов, восстановлением при высоких температурах парами бария галидов этих элементов, а в некоторых случаях и при восстановлении их окислов углем. Элементы подгруппы скандия представляют собой белые металлы с высокими температурами плавления и кипения. [38]
В химическом отношении элементы подгруппы скандия, в частности лантаноиды, очень близки между собой. Разделение их обычными методами - задача чрезвычайно трудная. [39]
При хроматографическом разделении элементов подгруппы скандия в качестве адсорбентов используются некоторые синтетические смолы. Поскольку соединения многих элементов этой подгруппы не имеют окраски, то зону нахождения их в колонке устанавливают по радиоактивности. Если природный элемент не радиоактивен, то в вещество, содержащее его, вводят соединения искусственно полученных радиоактивных изотопов данного элемента. [40]
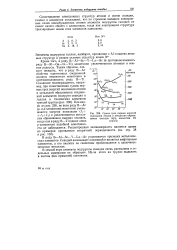 |
Сумма трех первых энергий ионизации атомов и энтальпии образования оксидов Э2О3 элементов III группы. [41] |
В земной коре элементы подгруппы скандия очень распылены и отдельных минералов не образуют. Из-за этого их трудно выделить в чистом ( без примесей) состоянии. [42]
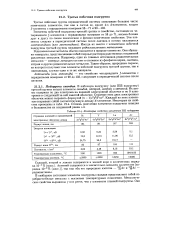 |
Некоторые свойства элементов ШБ подгруппы. [43] |
В свободном состоянии элементы подгруппы скандия представляют собой серебристо-белые металлы с высокими температурами плавления. Металлические свойства выражены у них резче, чем у элементов главной подгруппы. [44]
В свободном состоянии элементы подгруппы скандия представляют собой серебристо-белые металлы с высокими температурами плавления. Металлические свойства выражены у них резче, чем у элементов главной подгруппы. Они растворяются в разбавленных соляной, азотной и серной кислотах, а при нагревании реагируют с большинством неметаллов. [45]
Страницы: 1 2 3 4