3-атом
Cтраница 2
Наиболее часто связь индола с углеродом карбонила осуществляется за счет ( 3-атома ( бензальдегид [345] и его производные [355], ацетон [345]) но иногда и за счета-атома ( ацетальдегид [356]); реакции а-метилиндола с ацеталь-дегидом [356], ацетоном и гомологами, ацетофеноном [357] и антрахиноном [330] протекают, естественно, по первому типу. [16]
Если оба а-положения заняты СН3 - группами, то скорости обмена ( 3-атомов фурана и тиофена с раствором mpem - BuOK в ДМСО уменьшаются соответственно на два и на один порядок; резко ускоряется обмен с кислотой. [17]
В результате образования внутрирадикальной водородной связи происходит значительное увеличение константы расщепления на ( 3-атоме водорода с 3 6 Э в. [18]
Возможный механизм образования 3-атома состоит в связывании 1-атома с нормально связанным 2-атомом с образованием 3-атома и 2-атома; в итоге 1-атом переходит в 3-атом. Для этого требуется энергия Е3 - 2Е Е, где Е - электростатическая энергия дополнительного положительного заряда на 3-атоме. [19]
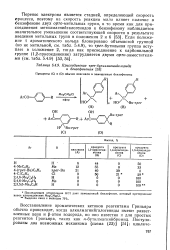 |
Присоединение трет-бутилмагнийхлорида к бепзофенонам. [20] |
Восстановление ароматических кетонов реагентами Гриньяра обычно происходит, когда алкилмагнийгалогениды имеют разветвленные цепи и ( 3-атом водорода, но оно известно и для простых реагентов Гриньяра, таких как н-бутилмагнийбромид. [21]
В возбужденном состоянии, как показано на приведенной выше схеме реакции, положительный заряд перемещен на 3-атом углерода, а отрицательный заряд - на карбонильный кислород. [22]
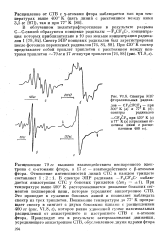 |
Спектры ЭПР фторалкильных радикалов - CF2CFCFj - при 300 К ( а и 77 К ( б. спектры радикалов. [23] |
Расщепление 79 гс вызвано взаимодействием неспаренного электрона с а-атомами фтора, а 17 гс - взаимодействием с 3-атомами фтора. При температуре выше 400 К растормаживается движение больших сегментов полимерной цепи, которые усредняют анизотропное СТВ. Это приводит к сужению боковых линий и позволяет наблюдать спектр из трех триплетов. Понижение температуры до 77 К превращает спектр в синглет с двумя боковыми пиками с расщеплением 400 гс ( рис. VI.8, г), которое равно удвоенной сумме максимальных расщеплений от анизотропного и изотропного СТВ с а-атомом фтора. [24]
По сравнению с соответствующими кислородными аналогами преимущества тиоловых эфиров в нуклеофильных реакциях по карбонильному атому углерода, в реакциях присоединения по ( 3-атому углерода а ( 3-ненасыщен-в: ых субстратов и в реакциях конденсации по углероду в а-положении к карбонильной группе достаточно очевидны. В каждом случае тиоловые эфиры оказываются более активными, чем их кислородные аналоги. [25]
Возможный механизм образования 3-атома состоит в связывании 1-атома с нормально связанным 2-атомом с образованием 3-атома и 2-атома; в итоге 1-атом переходит в 3-атом. Для этого требуется энергия Е3 - 2Е Е, где Е - электростатическая энергия дополнительного положительного заряда на 3-атоме. [26]
Кремнийорганические соединения, содержащие два и более атомов хлора в алкильной цепи, дегидрохлорируются значительно легче, чем монохлоралкилсиланхлориды; при этом отщепляется 3-атом хлора. При дегидрохлорировании а р-дихлоралкилсиланхлоридов хинолином образуется всегда одно соединение: а-хлор-а-алкенилсилаихлорид; дегид-рохлорирование р у-хлоралкилсиланхлоридов всегда сопровождается образованием двух соединений с различным положением кратной связи. [27]
Оказалось, что первой стадией этого превращения является обратимое образование Ав-производного ( GXVI) за счет mpawc - диаксиального отщепления 7а - оксигрушш и 6 3-атома трития. Далее это производное необратимо восстанавливается в ( CXVII) за счет транс-диэкваториального введения 6а - и 7р - атомов водорода. [28]
Из структурной формулы нафталина следует, что 8 атомов водорода этого углеводорода не равноценны и должны быть подразделены на две группы - на а - и 3-атомы. [29]
Нестереоспецифическое отщепление по реакции ( б) объясняется тем, что постулируется первоначальное образование диполяриого иона XXI, которое приводит к потере стереоспецифиче-ской конфигурации у ( 3-атома углерода. [30]
Страницы: 1 2 3 4