Замена - эфир
Cтраница 2
Однако более поздние работы той же школы54 показали, что успех применения диазометана как металирующего агента для многих гидроперекисей зависит от используемого растворителя. При замене эфира бензином или циклогексаном, реакция протекает бурно; через 1 5 ч кумилгидроперекись в циклогексане превращается в метилкумилперекись с выходом 77 %, а 18 7 % исходной гидроперекиси остается неизменной. Метил-1 - фенил-этил - и метилтетралилперекиси получаются аналогичным способом. Для метилирования гидроперекисей гексагидрофлуо-рена 10в и декагидропирена107 успешно применяется диазо-метан. [16]
При медленном испарении эфирного раствора кристаллы изогидробензоина I легко получить величиной до сантиметра и разделить их на зеркальные формы: таким образом Эрлен-мейеру в 1897 г. удалось получить оптически активный изо-гидробензоин с [ ос ] в 7 3, что составляет менее 10 процентов оптической чистоты. Лишь при замене эфира на этилацетат Риду в 1927 г. удалось добиться получения оптически чистых кристаллов. [17]
При медленном испарении эфирного раствора кристаллы изогидробензоина I легко получить величиной до сантиметра и разделить их на зеркальные формы: таким образом Эрлен-мейеру в 1897 г. удалось получить оптически активный изо-гидробензоин с [ аЬ 7 3, что составляет менее 10 процентов оптической чистоты. Лишь при замене эфира на этилацетат Риду в 1927 г. удалось добиться получения оптически чистых кристаллов. [18]
Из таблицы видно, что замена эфира тетрагидро-фураном позволяет в ряде случаев значительно повысить выход продуктов реакции. [19]
Присоединение натрия к соединениям с двойной связью, активированной сопряжением с ароматическими ядрами, имеет значение только как прием для получения соединений, содержащих в молекуле два атома натрия. Заметное влияние на развитие этой области оказала замена эфира как среды на эфиры этиленгликоля или тетрагидрофуран, в которых, в отличие от обычного этилового эфира аддукты растворимы. Это позволило более широко исследовать их реакции. [20]
Алкил-тиоэфиры, диэтилселенид и диметилтеллурид при образовании RMgX могут заменить эфир. Однако в их присутствии реакция не идет так гладко и они не имеют практич. Замена эфира на бензол, толуол, ксилол или петролейный эфир с добавкой небольшого количества этилового эфира обычно приводит к снижению выхода реактива Гриньяра. [21]
Алкил-тиоэфпры, диэтилселенид и диметилтеллурид при образовании RMgX могут заменить эфир. Однако в их присутствии реакция не идет так гладко и они не имеют практич. Замена эфира на бензол, толуол, ксилол или петролейный эфир с добавкой небольшого количества этилового эфира обычно приводит к снижению выхода реактива Гриньяра. [22]
Реактив Гриньяра приготовляют обычным путем из соответствующих бромистых ал-илов. Количество полученного реактива Гриньяра определяют иодометрически и добавляют необходимое количество хлористого кадмия. Замена эфира на бензол не является необходимой. Прибавляют требуемое уравнением количество этилового эфира пировиноградной кислоты, растворенной в эфире. Процесс протекает очень быстро, в конце реакционная смесь застывает в виде твердой массы. После нагревания в течение 3 - 4 час. [23]
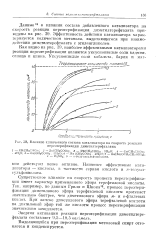 |
Влияние химического состава катализатора на скорость реакции переэтерпфпкацпп диметплтсрефталата. [24] |
Существенное влияние на скорость процесса переэтерпфпкацпп имеет характер применяемого эфира терсфталевой кислоты. Так, например, по данным Гриля и Шнока13, процесс переэтери-фпкации днметилового эфира терефталевоп кислоты протекает значительно быстрее, чем дпметилового эфира м - и о-фталевых кислот. При замене дпметилового эфира терефталевоп кислоты па диэтиловын эфир той же кислоты процесс переэтерифпкацип значительно замедляется. [25]
Вместо эфира можно применять третичные основания, причем образуются вещества типа аммониевых соединений. Челинцев [23] заменял эфир диметиланилином. Андрианов показал возможность [29] замены эфира на этиловый эфир ортокремневой кислоты. [26]
Как показал Малиновский [99], при более продолжительном нагревании паральдегида без предварительной деполимеризации с реактивами Гриньяра также образуются спирты. Выходы спиртов зависят от радикала магнийорганического соединения, и с увеличением числа углеродных атомов в радикале при прочих равных условиях понижаются. При замене эфира на бензол и нагревании при 70 - 80 С выходы значительно увеличиваются. Побочными продуктами являются кетоны, углеводороды и ацетали. [27]
Менее значительная детоксицирующая способность печени, несмотря на то что ферментативный путь детоксикации ФОС в печени наиболее выражен, связана, вероятно, с интенсивным окислением яда в пече-п И и активацией его в более токсичное соединение. Кроме того, определенную защитную роль играет лояная ХЭ плазмы крови. Значительная детоксикация происходит при взаимодействии яда с эритроцитами. Наименее выражена детоксицирующая способность в ткани мозга. Этот факт, а также высокая степень - угнетения ХЭ мозга изученными веществами, очевидно, играют решающую роль в токоикодинаиике ФОС и объясняют их значительную токсичность. Необходимо отметить, что замена лзопропилового эфира на этиловый приводит к тому, что ткани не обезвреживают яд в условиях эксперимента. [28]
Страницы: 1 2