Подобный заместитель
Cтраница 1
Подобный заместитель, независимо оттого, является ли он алкильной, карбоксильной или гидроксильной группой, будет называться в дальнейшем третично связанной или просто третичной группой, так как он находится у атома углерода, соединенного с тремя другими атомами углерода. [1]
Таким образом подобные заместители понижают энергию активации, необходимую для образования орто - н пара-продуктов замещения. [2]
Однако введение подобного заместителя в молекулу 2-оксибензо [ Ь ] тиофена не приводит к стабилизации еноль-иой формы. [3]
По данным ЯМР подобные заместители в центральной части молекул-алканов в заметных количествах отсутствуют. [4]
При наличии нитрогруппы и подобных заместителей мезомерный и индуктивный эффекты действуют в одном и том же направлении; введение нитрогруппы, особенно в пара-положение, резко увеличивает константу диссоциации. [5]
Расщепление основных азиридинов, имеющих подобные заместители во втором или третьем положении, также протекает весьма специфично. [6]
Учитывая механизм, при помощи которого подобные заместители ориентируют вступление нового заместителя, становится очевидным, что пара-положение дезактивируется сильнее, чем opmo - положение. [7]
Как правило, заместители в положениях 4 и 5 реагируют, как подобные заместители в бензольном ряду. [8]
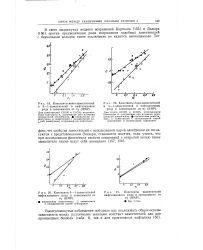 |
Константы жета-заместителей.| Константы лара-заместителей.| Константы 5 - 1-заместителей. [9] |
В свете выдвинутых недавно возражений Бартелла [155] и Дьюара [156] против преувеличения роли сопряжения подобных заместителей с бензольным кольцом такое заключение не кажется неожиданным. [10]
В этом случае ароматическое ядро должно быть очень активизировано к электрофильному замещению наличием NHg, ОН и подобных заместителей. [11]
В этом случае ароматическое ядро должно быть очень активизировано к электрофильному замещению наличием NHa, ОН и подобных заместителей. [12]
В органической химии хорошо известно, что цианистый водород, бисульфит натрия, аммиак и некоторые другие реагенты часто присоединяются по карбонильным двойным связям, но они редко реагируют с олефино-выми связями, если те не активированы сопряжением с карбонилом или подобным заместителем. К тому же реакции карбонильных соединений с электрофильными реагентами часто легко обратимы или ведут к последующим реакциям, причем образуются продукты, весьма отличные от продуктов простого присоединения. [13]
Если заместители проявляют - / и М - эффекты, то в положительно заряженном, а следовательно, сильноэлектрофильном о-комплексе преобладает донорное влияние, вытекающее из наличия свободной электронной пары. Таким образом, подобные заместители понижают энергию активации, необходимую для образования орто - и пара-продуктов замещения. [14]
Выясняется, что некоторые заместители в молекуле этилена чрез - - вычайно повышают как скорость полимеризации, так и ее степень. Интересно отметить, что при скоплении подобных заместителей склонность к полимеризации сильно уменьшается ( 1 1-дифенилутилон) или даже практически совершенно исчезает. Стилъбен на свету н бензольном растворе даст димер ( ср. [15]
Страницы: 1 2