Пересыщенный раствор
Cтраница 4
Пересыщенный раствор аналогичен переохлажденной жидкости и переохлажденному пару. [46]
Пересыщенный раствор по центральной трубе поступает в Кристаллизационную часть и поднимается вверх. Образовавшиеся кристаллы сульфата аммония распределяются по высоте кристаллизатора: большие кристаллы остаются внизу, средние - в средней части, а мелкие выносятся током жидкости в верхнюю часть. [48]
Пересыщенные растворы часто образуют вещества со сложной конфигурацией молекул. Хлорид серебра выпадает в осадок из пересыщенных растворов очень быстро, так как Ag и С1 - имеют сферическую форму и легко образуют центр кристаллизации. В противоположность этому ацетат натрия склонен к образованию пересыщенных растворов ввиду того, что низкая симметрия ацетатного иона затрудняет образование кристал лического зародыша. [49]
Пересыщенные растворы с концентрациями, соответствующими лабильной области, быстро кристаллизуются, в мета стабильной же области эти растворы то или иное время остаются без изменения. [50]
Пересыщенные растворы в обычных условиях могут долго сохраняться; кристаллизация возникает при введении затравки или механическом перемешивании, а также при ударе. Во время латентного периода кристаллизации возникшая твердая фаза не обнаруживается простыми оптическими средствами. Чтобы гидратиро-ванные ионы, скопившиеся в данном микрообъеме раствора, сблизились и образовали энергетически выгодные ассоциаты, необходимо создать определенные условия. При изучении нашей проблемы наибольший интерес представляет так называемый латентный ( индукционный) период, во время которого образуются зародыши кристаллов и происходит их рост до заметных размеров. [51]
Пересыщенные растворы, которые могут получаться при определенных условиях, также находятся в состоянии равновесия с окружающей средой. Однако, в отличие от рассмотренного выше случая, такое равновесие неустойчиво. Это проявляется в том, что при добавлении очень малого количества твердого вещества к пересыщенному раствору происходит выделение значительных количеств твердой фазы и раствор становится насыщенным. [52]
Пересыщенный раствор можно получить посредством испарения без существенного охлаждения в аппарате, который имеет характеристики испарителя. Такой аппарат рассчитывают, по существу, как испаритель, поскольку основная инженерная задача в обоих случаях определяется теплопередачей. При выпаривании раствора солей ( например, при осаждении NaCl из рассола в производстве поваренной соли) кристаллизация обычно сопутствует испарению, но особого контроля за размерами получаемых кристаллов не проводят. Кристаллизацию же, например, сахара осуществляют в вакуум-выпарном аппарате, но при этом ведут контроль за образованием правильных кристаллов. [53]
Пересыщенный раствор может быть получен также упариванием части растворителя. [55]
Пересыщенный раствор находится в крайне неустойчивом состоянии равновесия. Малейшее изменение его физического состояния сопровождается нарушением равновесия и выделением из раствора твердого вещества в кристаллическом виде. Такой процесс называется кристаллизацией. [56]
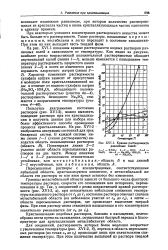 |
Кривые растворимости различных солей. [57] |
Пересыщенные растворы с концентрациями, соответствующими лабильной области, кристаллизуются мгновенно, в метастабильной же области эти растворы то или иное время остаются без изменения. [58]
Страницы: 1 2 3 4