Значение - атомные весы
Cтраница 3
Для приготовления различных растворов приходится вычислять необходимую навеску вещества; при этом прежде всего надо вычислить молекулярный вес вещества по атомным весам элементов. Значение атомных весов округляют до целых чисел, если подсчитывают величину навески для приготовления вспомогательного или титрованного раствора, точная концентрация которого затем будет установлена. В этом случае величину навески вычисляют, принимая во внимание только две значащие цифры, например 12 г, 4 2 г, и отвешивают вещество ( берут навеску) с соответствующей точностью. [31]
В Международных таблицах 1955 г. приведены значения атомных весов 36 элементов, полученные преимущественно или полностью на основании масс-спектроско-пических или ядерных данных. [32]
Из сопоставления с современной таблицей атомных весов следует, что для большей части элементов определения Берцелиуса выполнены с такой степенью точности, которая, принимая во внимание время и средства, имевшиеся в его распоряжении, достойна восхищения. Но при этом выявляется и несоответствие в отборе значений атомных весов, так как в некоторых случаях приведены величины, приблизительно вдвое большие, чем принятые ныне. [33]
Бегюэ де - Шанкуртуа в работе О естественной классификации простых тел или радикалов, называемой земным винтом ( 1863 г.) представляет систему элементов в виде спиральной линии, намотанной на поверхность цилиндра; основание цилиндра разделено на 16 равных частей, причем каждому такому делению, по мнению автора, должен соответствовать особый элемент, попадающий на соответствующее место на винтовой линии. На образующей же линии ( параллельной оси цилиндра) откладываются значения атомных весов. [34]
Вапстра [4148] вычислил атомные веса химических элементов по результатам измерений содержаний изотопов и массам их атомов. Результаты этих вычислений для большинства химических элементов практически совпадают со значениями атомных весов, рекомендованных в докладах. [35]
При этом в конце четного ряда около Си, Ag и Аи ставятся значения атомных весов, а в начале почетного ряда в скобках стоят лишь символы элементов. [36]
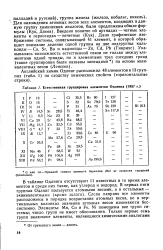 |
Естественная группировка элементов Одлинга ( 1857 г. [37] |
В таблице Одлинга отсутствуют 11 известных в то время элементов и среди них т акие, как углерод и водород. Слева направо все элементы расположены в порядке возрастания атомных весов, но в вертикальных колонках значения атомных весов изменяются бессистемно. Элементы: Мп, Со и Fe, Ni помещены вне групп системы; число групп не имеет обоснования. [38]
 |
Расположение химических элементов по октавам. [39] |
Во времена Менделеева значения атомных весов элементов были снова значительно уточнены, но все еще содержали такие ошибки, что установленная им последовательность расположения элементов оказалось правильной. На самом деле периодичность элементов непосредственно не связана с их атомными весами, но погрешность в значениях атомных весов была так велика, что это дало возможность Менделееву установить для них правильную последовательность, совпадающую с их порядковыми ( атомными) номерами. Современные значения атомных весов показывают, что существуют по крайней мере три пары элементов, последовательность расположения которых в периодической та блице не соответствует увеличению их атомных весов: кобальт и никель, аргон и калий, а также теллур и иод. Впрочем, Менделееву была известна аномалия пары теллур - иод, и все же он правильно поместил эти элементы в соответствующие им группы, основываясь в данном случае на их химических свойствах. Менделеев был твердо убежден, что при более тщательном определении атомный вес теллура окажется меньше, чем у иода. [40]
Так как использованные для расчетов относительных весов атомов анализы различных авторов были неточными, то и полученные Дальтоном значения атомных весов также оказались весьма неточными. В дальнейшем, однако, как мы увидим, Дальтон многократно пытался уточнить эти данные. [41]
В ближайшие годы после своей классической работы он пишет серию обзорных статей, посвященных определению атомных весов элементов периодической системы, в том числе и редкоземельных. В 1904 г. он проводит исследование над окисью гадолиния и уточняет величину его атомного веса; затем переоценке подвергаются значения атомных весов для эрбия и иттербия. [42]
Число известных хим. элементов превысило к этому времени 60, св-ва многих из них были достаточно хорошо изучены, а значения атомных весов определены с большей или меньшей точностью. [43]
А между тем весь дальнейший прогресс химии был связан именно с принятием молекулярной теории Авогадро-Жерара и вытекающих из нее новых ( истинных) значений атомных весов для многих ( но еще не всех. [44]
Приведенные в нем данные совпадают с числами, опубликованными в 1826 г., если не считать незначительных расхождений, появившихся в связи с тем, что значения атомных весов 1826 г., вычисленные с точностью до третьего з-нака, здесь округлены до второго знака, вследствие чего атомные веса относительно кислорода с атомным весом ( равным 16) также незначительно изменились. [45]
Страницы: 1 2 3 4