А-аминогруппа
Cтраница 3
 |
Разделение аминокислот ( а и тироидных гормонов ( б в виде К 0-диизопропил-производных Сорбент - силикон OV-17 на хро-мосорбе W-HP. [31] |
Структурные масс-спектрометрические исследования показали, что образуются изопропиловые эфиры, а к а-аминогруппе присоединяется только одна изопропильная группа. [32]
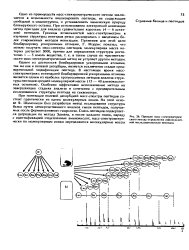 |
Принцип масс спектрометриче ского метода определения аминокислотной последовательности пептидов. [33] |
Одно из преимуществ масс-спектрометрического метода заключается в возможности анализировать пептиды, не содержащие свободной а-аминогруппы, и устанавливать химическую природу блокирующего остатка. При использовании электронной ионизации метод пригоден для анализа сравнительно коротких ( 4 - 6 остатков) пептидов. Границы возможностей масс-спектрометрии в изучении структуры пептидов резко расширились с введением более современных методов ионизации. [34]
Очень важно установить, образуется ли азот нитрильнои группы при биосинтезе этих циангидринов из а-аминогруппы фенилаланина или тирозина. [35]
Согласно первоначальным данным Браунштейна и Крицман, кетоглутаровая и щавелевоуксусная кислоты могут служить акцепторами а-аминогрупп многих аминокислот. [36]
Правда, метод обладает ограниченной специфичностью, так как динитрофторбензол реагирует не только с а-аминогруппами N-концевых аминокислот, но и с е-аминогруппами лизина, SH-группами цистина, ОН-группами тирозина и имидазольными группами гистидина. Рднако е - ДНФ-лизин легко отличить с помощью соответствующего свидетеля, а все остальные производи ные бесцветны и не мешают определению. [37]
Чтобы определить - аминокислоты в водном растворе по их карбоксильной группе, необходимо предварительно связать их а-аминогруппы, чтобы предотвратить образование внутренних солей, которые мешают титрованию. [38]
Если радикалы аминокислот нейтральные, то они почти не оказывают влияния на диссоциацию а-карбоксильной группы или а-аминогруппы, и величины рК ( отрицательный логарифм константы диссоциации) остаются относительно постоянными. Вследствие этого кривые диссоциации почти всех нейтральных аминокислот накладываются друг на друга и могут быть рассмотрены на примере аланина. [39]
Как видно из уравнения реакции, в образовании цветного продукта принимает участие азот аммиака, образующегося из а-аминогруппы. Таким образом, нингидриновая реакция выявляет свободные а-аминогруппы. Чем больше свободных а-аминогрупп содержит белок, тем интенсивнее окраска, образующаяся при взаимодействии его с нингидрином. [40]
Аналогичное рассмотрение показывает, что изоэлектрическая точка для лизина должна быть близкой к полусумме значений рКа для а-аминогруппы и е-аминогруппы. [41]
Этерификацию можно контролировать с помощью тонкослойной хроматографии, так как отсутствие реакции с нингид-рином указывает на ацилирование а-аминогруппы. Будучи полезной на первом этапе исследования, методика, однако, не является удовлетворительной для определения процента превращения малых количеств аминокислоты. Намного труднее поставить опыты для доказательства того, что вещество устойчиво на колонке, а площадь регистрируемого пика действительно отвечает известному количеству аминокислоты. Большинство исследователей довольствовалось предположением, что пик правильной формы измеряет все количество аминокислоты, нанесенной на колонку. Для того чтобы компенсировать потери, связанные с обработкой или различными условиями ввода пробы, необходимо включать внутренний стандарт. В пламенно-ионизационных детекторах молярная интенсивность сигналов для всех аминокислот различна, но линейность интенсивности сигнала в нормальных рабочих пределах позволяет проводить количественное измерение неизвестных соединений, поэтому между ними существует прямо пропорциональная зависимость. Для вычисления молярных соотношений ( например, в пептидном гидролизате) внутренний стандарт не требуется. Его нужно включать в одинаковой концентрации в стандартную анализируемую смесь в том случае, если нужно рассчитать абсолютное количество каждой аминокислоты ( см. разд. [42]
Титрование от рН 8 5 до рН 6 5 обусловлено взаимодействием протонов с имидазольными группами гистидина и с концевыми а-аминогруппами, которые присутствуют в белке в небольшом количестве. Аргинин при титровании непосредственно не определяется, так как константа диссоциации гуанидиновой группы настолько высока ( р / Сз несколько выше 13), что эта группа при любом значении рН, допускающем точные измерения, не может в заметном количестве перейти в ионизированную форму. Поэтому максимальное связывание основания белком нельзя определить достаточно точно. [43]
Недавно в качестве средства, дающего возможность различать эти два типа функциональных групп, Рейд [496] применил избирательное ацетили-рование свободных а-аминогрупп с последующей реакцией е-аминогрупп с ДНФБ. Он нашел, что ростостимулирующая и диабетогенная активность гормона роста зависит от наличия е-аминогрупп, но не концевых а-аминогрупп. [44]
Фирма Pharmacia поставляет сорбент Lysine-Sepharose 4B r в котором в качестве лиганда фигурирует закрепленный непосредственно на сефарозе через свою а-аминогруппу лизин. Этот сорбент представляет собой амфотерный обменник, несущий ионогенные группы обоих знаков, определенным образом взаимно ориентированные в пространстве. Плазминоген элюи-руют с сорбента с помощью е-аминомасляной кислоты, которая, по-видимому, выступает в качестве конкурирующего лиганда, а нуклеиновые кислоты - увеличением концентрации NaCl, что свидетельствует в пользу ионного характера их связи с остатками лизина. [45]
Страницы: 1 2 3 4