Суммарная скорость
Cтраница 2
Суммарная скорость многостадийного процесса определяется скоростью наиболее медленной стадии. Выявление этой стадии и является первым этапом изучения кинетики ионного обмена. [16]
Суммарная скорость ферментативной реакции определяется концентрацией фермент-субстратного комплекса. По закону действующих масс высокая концентрация субстрата сдвигает равновесие в сторону фермент-субстратного комплекса вплоть до такого состояния, когда все молекулы фермента окажутся связаны с субстратом в комплексе ES. Когда это произойдет, дальнейшее повышение концентрации субстрата уже не увеличивает концентрацию комплекса ES и, следовательно, не увеличивает скорости реакции. [17]
Суммарная скорость обратимой реакции может быть увеличена за счет избирательного отвода одного или нескольких продуктов из зоны реакции. [18]
Суммарная скорость каталитического процесса должна зависеть от скоростей его отдельных стадий и их соотношения. [19]
Суммарная скорость радикально-цепного процесса и кинетическая длина цепи, фактически определяющие выход при данных физико-химических условиях, зависят от скоростей реакций зарожде ния, развития и обрыва цепи ( см. гл. Скорость реакций зарождения цепи обычно можно регулировать подбором инициатора, температуры и других экспериментальных условий. Скорость реакций обрыва цепи не поддается прямому контролю, поэтому такие реакции являются серьезным ограничением процессов, текущих по радикально-цепному механизму. Если в течение такого короткого времени происходит большое число стадий развития цепи, то, очевидно, это является результатом малых концентраций радикалов ( их встречаТимеет значительно меньшую вероятность, чем встреча радикала и молекулы), а также результатом особенностей протекания реакций развития цепи. Количественно эти особенности, а также конкуренция между реакциями описываются на основании данных о равновесиях и константах скорости этих реакций. [20]
Суммарная скорость цепного превращения находится как сумма скоростей расходования отдельных компонентов. [21]
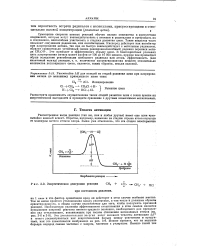 |
Энергетическая диаграмма реакции СН4. СЬ. [22] |
Суммарные скорости цепных реакций обычно сильно снижаются в присутствии соединений, которые могут взаимодействовать с атомами и радикалами и превращать их в соединения, неспособные участвовать в стадиях развития цепи. Такие вещества часто называют лопушками радикалов, или ингибиторами. Это приводит к эффективному обрыву цепи. В благоприятных условиях цепь хлорирования метана может пройти от 100 до 10 000 циклов, прежде чем произойдет обрыв вследствие рекомбинации свободного радикала или атома. [23]
 |
Схема г - / пере - тов Леггетта является то, что постоян-хода. Объяснения в тексте ство спектральной плотности р ( ш ( число уравнений на единичный интервал. [24] |
Суммарная скорость любого процесса определяется его самой медленной стадией. В случае химических реакций это значит, что появление конечного ( до диссипации энергии) химического продута совпадает с таким квантовым скачком, приводящим к мгновенному изменению конструкции электронной и ядерной системы. После этого энергия конечного химического состояния раньше или позже диссипирует. В случае радиоактивного распада это означает, что туннельный переход от частицы внутри ядра к соответствующему осциллятору совпадает с образованием свободной частицы. [25]
Суммарные скорости цепных реакций обычно сильно снижаются в присутствии соединений, которые могут взаимодействовать с атомами и радикалами и превращать их в соединения, неспособные участвовать в стадиях развития цепи. Такие вещества часто называют ловушками радикалов или ингибиторами. Это приводит к эффективному обрыву цепи. В благоприятных условиях цепь хлорирования метана может пройти от 100 до 10 000 циклов, прежде чем произойдет обрыв вследствие рекомбинации свободного радикала или атома. [26]
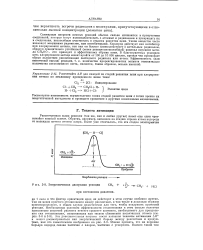 |
Энергетическая диаграмма реакции СН4. С1. [27] |
Суммарные скорости цепных реакций обычно сильно снижаются в присутствии соединений, которые могут взаимодействовать с атомами и радикалами и превращать их в соединения, неспособные участвовать в стадиях развития цепи. Такие вещества часто называют ловушками радикалов, или ингибиторами. Это приводит к эффективному обрыву цепи. В благоприятных условиях цепь хлорирования метана может пройти от 100 до 10 000 циклов, прежде чем произойдет обрыв вследствие рекомбинации свободного радикала или атома. [28]
Суммарная скорость катионной полимеризации прямо пропорциональна концентрации катализатора, а средняя степень полимеризации от концентрации катализатора не зависит, но прямо пропорциональна концентрации мономера: и & [ К ]; Р & [ М ], где [ К ] - концентрация катализатора; [ М ] - концентрация мономера. [29]
Суммарная скорость распада перекисей ацилов и эфиров над-кислот может зависеть от того, в каком растворителе проводится реакция. В первую очередь, это связано с возможностью проявления клеточных эффектов. Первоначально образовавшиеся радикалы могут рекомбинировать с образованием исходного соединения до того, как произойдет их диффузия из клетки растворителя. [30]
Страницы: 1 2 3 4