5-характер
Cтраница 1
Процент 5-характера СП-связи связан также с угловым напряжением: когда угол между связями у тетраэдрического атома углерода уменьшен благодаря включению этого атома в малый цикл, л-характер экзоциклической двойной связи С - Н возрастает. Следовательно, можно ожидать, что в ряду циклогексан-циклопеитан-циклобутан-циклопропан кислотность должна увеличиваться. [1]
Как видно из табл. 5.7, КССВ 2JH H увеличиваются с ростом 5-характера связи и электроотрицательности заместителей. [3]
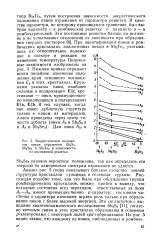 |
Энергетическое положение пиков отражения Sb2S3, Sb2Ses и SbYTea в зависимости от постоянной решетки. [4] |
Анализ рис. 5 снова показывает близкое сходство зонной структуры кристаллов сульфида и селенида сурьмы. AI-Ад, имеют преимущественно р-характер; состояния ч а стично 5-характера начинают играть роль только при образо вании пиков с более высокой энергией. Это согласуется с вы водами квантовохимического исследования Sb2S3 [11], согласно которым связи в этих кристаллах образованы в основном р-электронами с некоторой долей лр - гибридизации. [5]
Наиболее эффективное сопряжение пары электронов азота с бензольным кольцом будет наблюдаться тогда, когда эта пара располагается на / j - орбитали, параллельной р-орбиталям ароматической системы. Однако пара электронов азота стремится занять гибридную орбиталь с некоторым вкладом 5-характера, что энергетически предпочтительно. Для анилина реализуется компромисс, при котором неподеленная пара элпоронов азота занимает орбиталь с большей долей / - характера, чем в аммиаке, но имеющей все же некоторый вклад л-орбитали. [6]
Для тройной связи С - С в алкинах так же, как и для двойной углерод-углеродной связи в алкенах, характерны реакции электрофильного присоединения. Однако алкины вступают в них труднее, чем алкены. Это можно объяснить тем, что углерод-углеродные связи этинильной группы имеют больший 5-характер, и поэтому труднее атакуются электрофилом. [7]
Страницы: 1
