Соединение - атом - водород
Cтраница 2
 |
Нахождение энергии активации реакции между окисью азота и кислородом. [16] |
Можно положить, что длины связей N0 и О-О на рис. 72 равны соответственно 1 22 и 1 32 А, что близко к нормальным значениям, а расстояние N - О равно 5 А, по аналогии с расстоянием Н - Н в активированном комплексе, образующемся при соединении атомов водорода ( см. стр. Изменение этих величин, так же как и других, например частот колебаний, не может очень сильно влиять на удельную скорость; самые большие допустимые вариации их значений могут изменить конечный результат не больше, чем в 10 раз. [17]
Установлено, что образование молекулы при соединении атомов происходит в том случае, если общая энергия системы уменьшается. Так, при соединении атомов водорода в молекулу Н2 выделяется 431 Дж / моль теплоты на каждый моль водорода. Отсюда следует, что молекула водорода обладает меньшим запасом энергии, чем суммарная энергия его свободных атомов. [18]
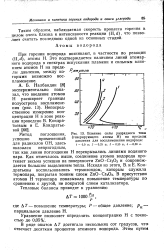 |
Влияние силы разрядного тока. [19] |
Метод поглощения, успешно примененный для радикалов ОН, здесь оказался непригодным, так как линии поглощения Н перекрывались линиями водяного пара. Как отмечалось выше, соединение атомов водорода протекает весьма успешно на поверхности ZnO Сг2О3 и сопровождается большим выделением тепла. [20]
Реакция прямого взаимодействия молекул водорода и хлора в их смеси практически не протекает из-за очень высокой энергии активации. Не обнаружены также реакции соединения атомов водорода и хлора с образованием хлороводорода. Это объясняется как низкими концентрациями атомов водорода и хлора, гак и тем, что энергия возникающей молекулы НС1, содержащая избыточные энергии атомов и энергию связи, очень велика, и эта молекула сразу же снова распадается на атомы. [21]
На этом основан способ сварки, предложенный Ланг-мюрдм и заключающийся в том, что струя атомарного водорода направляется на место соединения металлических частей. Вследствие выделения большого количества тепла при соединении атомов водорода Н в молекулы Н2 происходит местное расплавление металла и образование шва. При этом различают тримолекулярные ( три частицы), бимолекулярные ( две частицы) и мономолекулярные ( одна частица) реакции. [22]
Нуклеофильные соединения, с которыми они реагируют, - это полярные соединения, передающие пары электронов атому углерода в органических молекулах. Таким образом, алкилирование представляет собой замещение в нук-леофильиом соединении атома водорода алкильной группой, и весь процесс называется нуклеофильным замещением. [23]
Адкинс и Лазие [1, 2] нашли, что соотношение между дегидратацией и дегидрогенизацией не зависит от строения спирта, а зависит лишь от характера катализатора. Тейлор и Левин [24] установили, что чисто дегидратационный катализатор ускоряет, главным образом, соединение атомов водорода и гидро-ксильных радикалов, между тем как типичный дегидрогенизационный катализатор ускоряет соединение атомов водорода. [24]
Поскольку в структуре полиэтилена содержатся а-углеродные ( третичные) атомы, отличающиеся повышенной реакционной способностью, то образование гидроперекисных групп происходит, вероятно, в первую очередь у этих атомов. Однако большое разнообразие первичных продуктов реакции окисления модельных насыщенных соединений свидетельствует, что большинство содержащихся в этих соединениях атомов водорода, находящихся в различных положениях, имеет сравнимые реакционные способности [ 79, стр. [25]
В этом случае возможен любой из двух типов реакции, описанных выше, но реакция между радикалами в первом адсорбированном слое кажется более вероятной ввиду природы образующихся продуктов. Полимерный продукт, вероятно, образуется при реакции углеводородных радикалов в первом адсорбированном слое, тогда как удаление водорода может происходить при соединении атомов водорода в первом слое или, возможно, при взаимодействии адсорбированного атома водорода с молекулой во втором слое. Этот факт и то, что на силикагеле реакция в целом протекает до конца значительно быстрее, можно считать указанием на то, что энергия активации реакции между радикалами R - ниже в том случае, когда они адсорбированы на силикагеле, чем когда они адсорбированы на угле. [26]
Адкинс и Лазие [1, 2] нашли, что соотношение между дегидратацией и дегидрогенизацией не зависит от строения спирта, а зависит лишь от характера катализатора. Тейлор и Левин [24] установили, что чисто дегидратационный катализатор ускоряет, главным образом, соединение атомов водорода и гидро-ксильных радикалов, между тем как типичный дегидрогенизационный катализатор ускоряет соединение атомов водорода. [27]
Согласно этой теории, перенапряжение возникает вследствие накопления атомов водорода на поверхности катода, и изменение перенапряжения при переходе от одного металла к другому приписывается различному каталитическому воздействию этих металлов на скорость соединения атомов водорода в молекулы. Металлы с низким перенапряжением, например платина, палладий, никель и медь, должны быть хорошими катализаторами для реакции 2Н Н2, между тем как металлы с высоким перенапряжением, например свинец, ртуть, олово и кадмий, должны были бы оказаться плохими катализаторами для той же реакции. [28]
Поэтому исследователю трудно различить, является ли наличие тяжелого водорода в соединении результатом химической реакции, катализируемой определенным ферментом, или же следствием обычного водородно-дейтериевого обмена. Однако не все атомы водорода в молекулах могут легко обмени ваться. Соединение атомов водорода и углерода является проч ным, поэтому связь дейтерия с углеродными цепями является результатом исключительно метаболических реакций. [29]
Эффект несминаемой отделки, полученный в результате обработки целлюлозного материала продуктом предварительной конденсации мочевины с формальдегидом, после многократных стирок практически исчезает. Разработка новых типов сшивающих агентов, в частности циклических производных мочевины, была вызвана стремлением решить проблему устойчивости достигаемого эффекта к указанным обработкам. Однако наличие в этих соединениях атома водорода у азота в N-оксиметилпроизводных может привести к образованию хлор-амида при отбеливании растворами гипохлорита. [30]
Страницы: 1 2 3