Измерение - потенциал
Cтраница 1
Измерение потенциала следует проводить вслед за отключением тока через небольшой промежуток времени ( 150 - 400 мс), необходимый для исключения влияния переходных процессов. Uoff; Uaus в зарубежной литературе) и это значение во многих случаях близко к величине поляризационного потенциала. В настоящее время отечественная промышленность выпускает приборы ПКО и Поиск-01, предназначенные для этих целей. [1]
Измерение потенциала на различных участках поверхности катода затруднительно, так как величина его из-за движения поверхности неустойчива. Однако в среднем разность потенциалов на лицевой ( у стенки стеклянной трубки) и обратной стороне капли - катода составляет около 0 5 вольт. Восстановление йодистого этила из водных и водноспир-товых растворов сопровождается газовыделением - согласно принятой схеме реакции выделяется этан. Поэтому электролиз йодистого этила проводился в растворе метилового спирта, в этом случае газовыделение отсутствует. В перетекающем растворе установлено наличие иодид-ионов, другие продукты не анализировались. [2]
Измерения потенциалов проводят в лабораторных исследованиях, а также в реальных условиях, если заранее известна зависимость скорости коррозии от потенциала, напр, для выбора и контроля катодной и анодной защиты мсталлич. Поляризационные кривые используются для установления механизма коррозии, для ускоренного определения устойчивости нек-рых сплавов против пит-тинговой коррозии и в нек-рых случаях для определения скорости коррозии. [3]
Измерение потенциала, возникающего на электродах, производится измерительным блоком рН - метра. [4]
Измерение потенциалов медного и цинкового электродов необходимо провести как для соответствующих 1 М, так и для Э 1 М растворов. Соединительным раствором между электродами и в этом случае является насыщенный хлорид калия. [5]
Измерения потенциалов и токов течения ( в принципе и электроосмоса) возможны не только в капиллярах и капиллярных системах, но и на плоских макроповерхностях. [6]
Измерения потенциалов и токов течения ( в принципе, и электроосмоса) возможны не только в капиллярах и капиллярных системах, но и на плоских макроповерхностях. [7]
Измерение потенциала производят в стандартном буферном растворе. [8]
Измерения потенциалов при кинетических исследованиях могут быть проведены и при использовании водных электродов сравнения, например хлорсеребряного, каломельного или водородного. Однако в этом случае потенциал-может быть измерен лишь с точностью до диффузионного потенциала, обусловленного разными активностями электролита в воде и органическом растворителе. Кроме того, при этом возникает необходимость предотвращения попадания воды в органический растворитель, что может быть осуществлено включением промежуточных сосудов с органическим растворителем и дополнительных закрытых кранов. [9]
Измерения потенциалов и токов течения ( в принципе и электроосмоса) возможны не только в капиллярах и капиллярных системах, но и на плоских макроповерхностях. [10]
Измерения потенциала в газовой фазе возможны с использованием электродов сравнения Na / стекло или платина в расплаве кислородсодержащих солей. [11]
Измерения потенциала и силы максимального тока, производимые непосредственно на экране осциллографа, позволяют судить, какие вещества и в каком количестве находились в растворе. [12]
Измерение потенциала, возникающего на электродах, производится измерительным блоком рН - метра. [13]
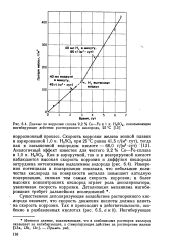 |
Данные по коррозии сплава 9 2 % Со-Fe в 1 и. H2SO4, показывающие ингибирующее действие растворенного кислорода, 25 СС. [14] |
Измерения потенциала и поляризации показали, что небольшие количества кислорода на поверхности металла повышают катодную поляризацию, снижая тем самым скорость коррозии; в более высоких концентрациях кислород играет роль деполяризатора, увеличивая скорость коррозии. [15]
Страницы: 1 2 3 4