Измерение - энтальпие
Cтраница 1
Измерения энтальпий таких реакций могут проводиться в любых калориметрах, рассмотренных в § 2 данной главы. Специфическим для них является только способ введения в калориметрическую жидкость газообразного реагента. [1]
Измерение энтальпий хлорирования веществ проводят в калориметрической практике значительно реже, чем измерение энтальпий сгорания в кислороде. Вызывается это в основном меньшей по сравнению с кислородом доступностью чистого хлора и тем, что работа с этим реагентом связана со значительно большими трудностями в отношении защиты деталей аппаратуры и коммуникаций от коррозии, чем работа с кислородом. [2]
Измерение энтальпий сожжения интерметаллических соединений обычно проводят для определения энтальпий их образования. [3]
Измерение энтальпий фторирования твердых веществ связано со значительно большими трудностями, чем измерение энтальпий сгорания в кислороде и энтальпий хлорирования. Определяется это очень высокой реакционной способностью фтора. [4]
Измерение энтальпий разложения твердых веществ встречается в калориметрической практике довольно часто. [5]
Для измерения энтальпий смешения служат специальные калориметры ( см. подробнее в [143]), которые должны быть герметичными, обладать высокой чувствительностью и иметь приспособление для эф активного перемешивания жидкостей. [6]
Методика измерений энтальпий фторирования имеет много общего с методикой измерений энтальпий сгорания в кислороде и энтальпий хлорирования. Основные отличия вызываются значительно большей агрессивностью фтора. Последнее обстоятельство требует очень внимательного контроля за возможностью появления побочных тепловых эффектов в результате реакции фтора с отдельными деталями аппаратуры. [7]
Условия измерений энтальпий различных процессов также существенно различны. [8]
При измерении энтальпий разбавления и смешения растворов часто приходится встречаться с большими затруднениями. Главным из них является то, что тепловые эффекты этих процессов в большинстве случаев очень малы и поэтому для их измерения требуются калориметры с очень высокой чувствительностью. Обычно при проведении эксперимента в калориметре приходится смешивать большое количество жидкостей; это усложняет конструкцию калориметров. Кроме того, очень важным является то, что при смешении меняется давление насыщенного пара в находящейся над жидкостью газовой фазе. Следствием этого являются процессы испарения или конденсации, а это может вызывать значительные ошибки. Наилучшим способом преодоления этого затруднения является использование калориметров, в которых газовой фазы над смешиваемыми жидкостями нет. Однако в ряде случаев используют и калориметры, в которых газовая фаза над смешиваемыми жидкостями имеется. [9]
 |
Калориметр Лейчера с сотрудниками. [10] |
Большое число измерений энтальпий хлорирования, бромирования и гидробромироваиия непредельных углеводородов и галоидированных углеводородов проведено начиная с 1949 г. Лейчером с сотрудниками. [11]
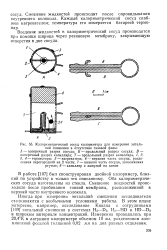 |
Калориметрический сосуд калориметра для измерения энтальпий смешения в отсутствие газовой фазы. [12] |
Иногда при измерении энтальпий смешения исследователи сталкиваются с необычными условиями работы. В этом плане интересно, например, исследование Кнаапа с сотрудниками [109] энтальпий смешения в системах Н2 - D2, H2 - HD и HD - D2 в широком интервале концентраций. [13]
Аналогично при измерении энтальпий смешения чистых жидкостей ( а не растворов) расчет величины энтальпии смешения может производиться как на сумму молей обоих смешиваемых компонентов, так и на количество молей любого одного из них. Все эти варианты расчета имеют практическое значение в зависимости от цели работы. [14]
Но работ по измерению энтальпий хлорирования этих веществ пока еще очень мало. [15]
Страницы: 1 2 3 4