Избыточный анион
Cтраница 1
 |
Схема образования двои - CNS - b либ образовывать С иона-ного электрического слоя в про - ми решетки трудно растворимые цессе первичной адсорбции. соединения ( правило Фаянса - Па. [1] |
Избыточные анионы в растворе ( в данном примере - - МОз), оставшиеся без партнеров, подтянутся к адсорбированным ионам Ag, вследствие кулоновского взаимодействия. Таким образом, на границе раздела фаз образуется ДЭС ( рис. 68 6), подобный конденсатору. По аналогии с конденсатором вводится понятие внутренней обкладки - находящейся в поверхностном слое со стороны твердой фазы, и внешней обкладки - со стороны жидкой. [2]
Избыточные анионы в растворе ( в данном примере - МОз) оставшиеся без партнеров, подтянутся к адсорбированным ионам Ag, вследствие кулоновского взаимодействия. Таким образом, на границе раздела фаз образуется ДЭС, подобный конденсатору. По аналогии с конденсатором вводится понятие внутренней обкладки - находящейся в поверхностном слое со стороны твердой фазы, и внешней обкладки - со стороны жидкой. Ионы, составляющие внешнюю обкладку называются противоионами. [3]
Избыточные анионы в растворе ( в данном примере - МОд) оставшиеся без партнеров, подтянутся к адсорбированным ионам Ag, вследствие кулоновского взаимодействия. Таким образом, на границе раздела фаз образуется ДЭС, подобный конденсатору. По аналогии с конденсатором вводится понятие внутренней обкладки - находящейся в поверхностном слое со стороны твердой фазы, и внешней обкладки - со стороны жидкой. Ионы, составляющие внешнюю-обкладку называются противоионами. [4]
Избыточные анионы С1 - в растворе, оставшиеся без партнеров, вследствие кулоновского взаимодействия подтянутся к адсорбированным ионам Mg2 н образуют подобно конденсатору, на границе раздела фаз ДЭС с внутренней обкладкой, находящейся в поверхностном слое со стороны твердой фазы, и внешней обкладкой со стороны жидкости. [5]
 |
Лиоэлектря - [ IMAGE ] Ионогенный двои - Ряс. 63. Адсорбцяон-чеокий двойной слой ной слой. ный двойной слой. [6] |
Внешняя же обкладка образуется избыточными анионами раствора. Такой двойной слой является по существу также адсорбционным. [7]
Поскольку кристалл электронейтрален, то наличие катионных вакансий или избыточных анионов в междоузлиях ( рис. 26.2, а, г) должно компенсироваться тем, что некоторые катионы в узлах решетки имеют больший заряд, чем остальные. [8]
Захват электрона ионом серебра приводит к образованию атома серебра и созданию местного отрицательного заряда в виде избыточного аниона на внешней поверхности или избыточного иона галоида, занимающего излом или неровность вдоль линии дислокации. Захват дырки ионом галоида приводит к образованию атома галоида и оставляет местный положительный заряд, обусловленный избыточным щелочным ионом на внешней поверхности, изломе или неровности. Созданные таким путем объемные заряды нейтрализуются подвижными ионами серебра, но до момента нейтрализации эти заряды могут сыграть роль ловушки для электронов или дырок, ранее захваченных другими ловушками, что может привести к рекомбинации. [9]
При этом твердая фаза приобретает положительный заряд, жидкая - отрицательный. Избыточные анионы в растворе ( в данном примере - NO), оставшиеся без партнеров, подтянутся к адсорбированным ионам Ag вследствие кулоновского взаимодействия. Таким образом, на границе раздела фаз образуется ДЭС, подобный конденсатору. По аналогии с конденсатором вводится понятие внутренней обкладки, находящейся в поверхностном слое со стороны твердой фазы, и внешней обкладки - со стороны жидкой. [10]
Равновесию Fe 3 e Fez отвечает определенная толщина двойного электрического слоя. Раствор заряжается отрицательно из-за избыточных анионов, а платина положительно. Величина скачка потенциала является мерой окислительной способности раствора. Редокс-электрод получают погружением платиновой пластины в раствор, содержащий одновременно любые окисленные и восстановленные формы, когда создаются системы: Н, PbOz, РЬ2, ( Pt); Н, MnO4 -, Mn2 ( Pt), Cr, Cr2 ( Pt) и другие, составленные по такому же принципу. Окислительно-восстановительные электроды отличаются от других, рассмотренных ранее, тем, что продукты окисления и восстановления остаются в растворе, а не выделяются на электроде. [11]
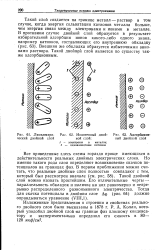 |
Лиоэлектри - [ IMAGE ] Ионогенный двои - [ IMAGE ] Адеорбцяон-ческий двойной слой ной слой. ный двойной слой. [12] |
Такой слой создается на границе металл - раствор в том случае, когда энергия сольватации катионов металла больше, чем энергия связи между электронами и ионами в металле. Внешняя же обкладка образуется избыточными анионами раствора. Такой двойной слой является по существу также адсорбционным. [13]
 |
Модель образования двойного электрического слоя на аноде.| Модель образования двойного электрического слоя на катоде. [14] |
Если силы гидратации меньше энергии связи между ион-атомами и электронами ( w Wi), то возникает двойной слой иного характера. Катионы раствора, в некотором количестве адсорбируясь на поверхности металла, образуют положительную внутреннюю обкладку двойного слоя; роль внешней обкладки будут играть избыточные анионы раствора, выстроенные в-ряд у поверхности вследствие электростатического взаимодействия. Расположение обкладок двойного слоя ( рис. 1 - 3) здесь обратно предыдущему: металл заряжается положительно, а раствор отрицательно. [15]
Страницы: 1 2