Кислородсодержащий анион
Cтраница 1
Кислородсодержащие анионы уступают им по силе. [1]
Кислородсодержащие анионы S0 -, CrO -, MnOj и СЮ обладают способностью химически адсорбироваться на пассивном железе, проникая в глубь пассивирующей окисной пленки, стабилизируя ее структуру и повышая защитные свойства. При этом не происходит существенного изменения термодинамических свойств, а следовательно, и химической природы пассивирующих окислов и их реальной способности вступать в те или иные окислительно-восстановительные электрохимические реакции. Перхлорат-ион обладает наивысшей адсорбционной способностью. Указанные анионы почти не влияют на стационарную скорость растворения железа, покрытого неповрежденной пассивирующей пленкой; лишь CrOJ несколько ее понижают. Стабилизация структуры пленки проявляется прежде всего в резком сокращении числа дефектных мест пленки и уменьшении их анодной активности. Этот эффект возникает в первую очередь, заметно опережая наступление общего стационарного состояния пленки. Следовательно, адсорбционный процесс развивается прежде всего на дефектных местах и лишь затем - постепенно охватывает всю массу пленки. Ионы СЮ, в отличие от остальных изученных анионов, обладают способностью проникать сквозь всю толщу пленки и прочно адсорбироваться на поверхности металла - внутренняя адсорбция. Этот процесс развивается медленно ( десятки минут) и затрагивает вначале лишь отдельные участки металла, число и площадь которых определяются топографией дефектности пленки. [2]
 |
Подпрограммы растворов, содержащих ионы ванадия ( V и железа ( II и III, и схематическое изображение кривых титрования ванадия ( V раствором соли Мора в различных условиях. [3] |
Кислородсодержащие анионы - перманганат, би-хромат и ванадат, имеющие большое применение в практике амперометрического титрования, восстанавливаются на электроде необратимо. Это значит, что если в растворе присутствуют одновременно окисленная и восстановленная формы, например Сг2С7 - и Сгш, то непрерывной катодно-анодной волны, подобной тем, которые были изображены выше ( см. рис. 14 и 15), получить нельзя. [4]
Кислородсодержащие анионы или не способны окисляться, или их окисление происходит при очень высоких потенциалах. [5]
Кислородсодержащие анионы брома методами ПТ определяют сравнительно редко, предпочитая визуальное титрование, хотя иногда потенциометрия обеспечивает выигрыш правильности результатов [610, 790] или чувствительности. [6]
Простые кислородсодержащие анионы элементов окрашены только в редких случаях. [7]
Некоторые кислородсодержащие анионы ( гидроокиси хромат-ных, азотнокислых и сернокислых солей) ингибируют точечную коррозию за счет вытеснения ионов СГ с поверхности. При определенном отношении 5ОГ / СГ точечная коррозия сталей не возникает. [9]
Многие кислородсодержащие анионы также способны к электрохимическому восстановлению на платиновом электроде. [10]
Большинство кислородсодержащих анионов ( СОз2 -, PCV, NCh, SO42, C1CV) не окисляются на аноде. [11]
 |
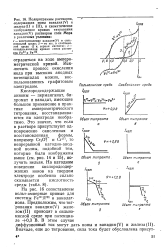
Полярограммы растворов ванадата аммония, бихромата и перманганата калия, снятые на платиновом вращающемся электроде. [12] |
Восстановление кислородсодержащих анионов протекает на платиновом электроде различно. На рис. 23 приведены вольт-амперные кривые для ванадата аммония, бихромата и перманганата калия. [13]
Известно, что кислородсодержащие анионы СгО - и MnOj способствуют пассивации железа, а анион C10J в определенных условиях, наоборот, активирует его. Ниже приведены результаты исследования индивидуального и совместного действия этих анионов на кинетику растворения железа в пассивной области, а также обсужден механизм наблюдавшихся явлений. [14]
Рассмотрим теперь влияние кислородсодержащих анионов на динамику растворения углеродистой стали. Выше было показано, что способность стабилизировать пассивную пленку, снижать ее дефектность у сульфат-ионов в кислом растворе выражена довольно слабо. Для определения влияния других анионов в 0 5 М раствор серной кислоты после 2-часовой выдержки электрода быстро вводили дополнительное количество раствора изучаемого электролита в серной кислоте. Раствор все время интенсивно перемешивался током очищенного азота. [15]
Страницы: 1 2 3 4
