Галоидный анион
Cтраница 1
Галоидные анионы продвигаются но пластинке в виде аммонийных солей, в то время как щелочные катионы остаются на старте. [1]
Поверхностная активность галоидных анионов возрастает в ряду: F - Cl-Br-J - так же, как и во всех растворителях, исследованных до настоящего времени. Подъем С - ср-кривых в анодной области для указанных анионов имеет одинаковый наклон ( рис. 1, кривые /, 5, 7, 8) и отличается от наклона кривых всех других анионов. [2]
В результате быстрого процесса фотоперехода сольватиро-ванный галоидный анион, Х - aq, переходит в новое качество - возбужденное образование, в котором радикал X окружен средой с сохранившейся в неизменности ориентационной поляризацией. [3]
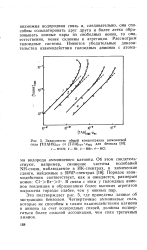 |
Зависимость общей концентрации аммониевой соли ( ТЛАНХ ] 0рг от [ ТЛА ] 0рг аНх Ддя бензола. [4] |
В связи с этим у галоидных анионов тенденция к образованию более высоких агрегатов выражена гораздо слабее, чем у ионных пар. [5]
Окисляющее действие галоидов обусловливается превращением нейтрального галоида в галоидный анион. [6]
В очень агрессивных условиях - при повышении концентрации галоидных анионов и температуры, следует использовать титан, являющийся из доступных конструкционных металлов наиболее стойким к питтинговой коррозии. [7]
Известно, что в окислительных средах в присутствии галоидных анионов легко пассивирующиеся металлы подвергаются местному-разрушению. В результате местного активирования поверхности коррозия развивается в отдельных центрах в виде глубоких поражений, называемых питтингами. Этому виду коррозии подвержены коррозионностойкие стали, алюминиевые, титановые и другие сплавы. [8]
В анодном растворении олова в спиртовых растворах принимают непосредственное участие галоидные анионы и молекулы растворителя. Данных для установления механизма растворения недостаточно. [9]
Из катионов в большей степени способствуют возникновению питтинга в присутствии агрессивных галоидных анионов окислительные металлические ионы трехвалентного железа, двухвалентной меди, двухвалентной ртути. Галоидные неокислительные соли Al, Ca, Na, хотя и вызывают питтинговую коррозию, но в меньшей мере, чем окислительные соли. Наличие в растворе Н СЬ кислорода и других окислителей является необходимым условием возникновения питтинговой коррозии, что вызвано их деполяризующим действием. [10]
Из катионов в большей степени способствуют возникновению питтинга в присутствии агрессивных галоидных анионов окислительные металлические ионы: трехвалентного железа, двухвалентной меди, двухвалентной ртути. Галоидные неокислительные соли таких катионов как Al, Ca, Mg, хотя и вызывают питтинговую коррозию, но в меньшей мере, чем соли с окислительными катионами. [11]
Алюминий весьма чувствителен, особенно в кислых средах, к галоидным анионом С1 -, F -, Br -, 1 -, разрушающим пассивную пленку. Наоборот, окислительные ионы типа хроматов или бихроматов, а также растворимые соли кремниевой кислоты и фторосиликаты являются сильными замедлителями ( ингибиторами) коррозии алюминия. [12]
Точечная коррозия на металлах, как правило, возникает в растворах, содержащих галоидные анионы, из которых наиболее агрессивны СГ и В г, в то время как F - точечную коррозию вообще не вызывает, обеспечивая значительное и равномерное растравливание поверхности металла. Точечная коррозия происходит, если концентрация галоидного иона равна критической концентрации, зависящей от природы металла и некоторых других факторов, или превышает ее. Увеличение концентрации галоидных ионов облегчает питтингообразование. [14]
Колотыркина и Л. И. Фреймана [55] по исследованию железа в нейтральных водных растворах, содержащих галоидные анионы, показали, что Ет зависит от концентрации галогена и его вида. [15]
Страницы: 1 2
