Кислородный анион
Cтраница 3
Простейшим допущением является предположение, что основные направления упаковки совпадают с направлениями координатных осей кристалла. В случае рамзаита 36 кислородных анионов, приходящихся на ячейку, требуется подразделить на определенное количество рядов и слоев. [31]
Рассмотренная гипотеза, согласно которой катион металла является основным активным центром катализатора, не учитывает роль кислородных анионов. Возможно, что роль кислородных анионов заключается в их превращении в гидроксильныи ион в результате взаимодействия с водородом исходного углеводорода; в этом случае образующийся алкилышй радикал может взаимодействовать с катионом металла, соединяясь с ппм, как указывалось выше. По-видимому, такая реакция протекает на поверхности катализатора, даже если в основном ядре фазы подобное восстановление невозможно. [32]
Добавление модифицирующих окислов к кремнезему приводит к разрыву мостиковых связей кремний - кислород. Считают, что связанный с вводимым кислородным анионом отрицательный заряд ( - 2) равномерно распределен между двумя соседними тетраэдрами SiO4, которые разделяют этот анион. Таким образом, на каждом тетраэдре существует отрицательный заряд - 1, который может быть локализован на немостиковом атоме кислорода или равномерно распределен в тетраэдре между четырьмя атомами кислорода. Схема, иллюстрирующая соединяются два катиона. [33]
В соответствии с теорией электронной конфигурации, разрабо - - Танной Улигом, склонность никеля к пассивированию основана на действии незаполненной Suf-оболочки никеля. Как переходный элемент он способен хемосорбировать кислородные анионы. [34]
По существу, всегда присоединяется сульфит SO3, нуклеофильность которого настолько велика, что бензальдегид реагирует с ним примерно в 10000 раз быстрее, чем с бисульфитом. Бисульфит, по-видимому, необходим лишь для протежирования кислородного аниона, образующегося промежуточно из карбонильного кислорода. Этот процесс препятствует обратной реакции - распаду на исходные компоненты. [35]
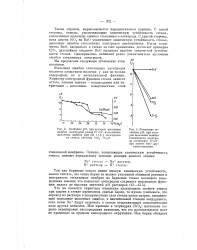 |
Величина рН, при которой щелочная.| Изменение величины рН, при которой щелочная ошибка стеклянного электрода составляет 10 mV, при замене ВаО другими окислами. [36] |
Что же касается характера изменения электродных свойств стекол при замене в стекле кремнезема окисью бария, то нужно учитывать, что переход из раствора в поверхностные слои стекла ионов натрия, вызывающий появление щелочных ошибок, в значительной степени затруднится, если ионы Na будут встречать в стекле отталкивающее положительное поле других катионов. Ион кремния в тетраэдрах [ Si04 ] настолько хорошо экранирован кислородными анионами, что его положительное поле не проникает за пределы кислородного окружения. [37]
Сопоставление с литературными данными, а также анализ параметров спектров ЭПР показывают, что ионы IA соответствуют пентааммиакатам. Таким образом, при адсорбции аммиака на гидратированных образцах происходит максимальное замещение кислородных анионов на молекулы аммиака в координационной сфере иона Сп2 по сравнению с дегидратированными цеолитами, что свидетельствует о более прочном связывании ионов Сп2 с каркасом цеолита в дегидратированных образцах по сравнению с гидратирован-ными. В этом случае после адсорбции аммиака компенсация заряда решетки цеолита осуществляется катионами NH4, а гидроксильные группы вытесняются молекулами аммиака во вторую координационную сферу. [38]
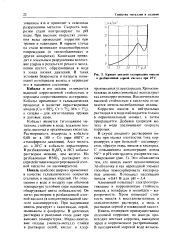 |
Кривая анодной поляризации ннкели в разбавленной серной кислоте при 25 С. [39] |
В случае анодного растворения никель при малых плотностях тока корродирует, а при большой - пассивируется, образуя окись никеля и кислород. Это объясняется тем, что никель имеет незаполненную Зс1 - оболочку и как переходной элемент способен хемосорбировать кислородные анионы. [40]
Таким образом, кислород в большинстве случаев в своих соединениях находится на 2 - й ступени восстановления. Однако не следует думать, что целое число, обозначающее номер ступени, имеет значение для понимания истинного заряда кислородных анионов и заряда присоединенных катионов. [41]
Известно [1-3], что во многих технических стеклах и эмалях физико-химические свойства зависят от кислотно-основных ха -, рактеристик расплавов, определяемых соотношением основных и кислотных окислов. Введение в стеклообразные системы кислотных окислов с большой силой единичной связи катиона с кислодором ( SiOj, В2Оз, РаОе и др.) понижает активность кислородных анионов и повышает степень жесткости кремнекисло-родного каркаса. Последнее подтверждается улучшением химических и механических показателей синтезируемых стекол и эмалевых покрытий. [42]
Известно, что свободные кислородсодержащие кислоты, как правило, менее стабильны, чем большинство их солей. Это объясняется, во-первых, очень сильным поляризующим действием Н, и, во-вторых, иным характером контрполяризации. Протон, внедряясь в кислородный анион, снижает его заряд и уменьшает деформируемость, поэтому НСОз и НЗОз менее устойчивы, чем, соответственно, СОз - и SOJT. Второй протон делает частицу еще менее устойчивой, поэтому и Н2СО3, и ШЗОз легко теряют воду. Это является также одной из причин того, что кислородсодержащие кислоты - более сильные окислители, чем их соли. [43]
Максимум плотности при 18 % борной кислоты отвечает в этом случае минимуму поляризуемости, которая вызывается комбинированными действиями сокращения объема и молекулярной ассоциации. Хамфрис и Морган118 исследовали влияние термической истории на диэлектрические постоянные и плотности натриево-боро-силикатных стекол. Конституционные воздействия химического состава выражаются главным образом в изменении отношения числа кислородных анионов к сумме чисел катионов кремния и бора, которое определяет число кислородных ионов, связанных только с одним катионом. Эти кислородные ионы вызывают уменьшение плотности и увеличение диэлектрической постоянной и показателя светопреломления. [44]
При температуре 1000 С такие электролиты обладают довольно высокой проводимостью ( обычно в пределах 10 - 0 1 См / м) по отрицательно заряженным ионам кислорода. Проводимость примесных электролитов проходит через максимум при содержании добавки в интервале 5 - 15 мол. Падение проводимости при большом содержании добавки вызвано образованием комплексов между катионами добавки и кислородными анионами. Проводимость-этого класса электролитов зависит также от природы добавки. Максимальная проводимость оказывается обычно тем выше, чем меньше радиус катиона добавки. [45]
Страницы: 1 2 3 4