Увеличение - энтропия - система
Cтраница 1
Увеличение энтропии системы в результате необратимости адиабатного процесса в насосе подсчитывается следующим образом. [1]
Увеличение энтропии системы при протекании в ней необратимых процессов иногда называют производством энтропии. [2]
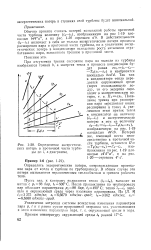 |
Определение эксергетических потерь в проточной части турбины по (, s - диаграмме. [3] |
Увеличение энтропии системы вследствие изменения параметров пара р, i и s равно сумме Приращений энтропии тел. [4]
Увеличение энтропии системы означает переход в состояние, имеющее большую вероятность. [5]
Полученное неравенство показывает увеличение энтропии системы при необратимом теплообмене между телами. [6]
Однако согласно (6.2) увеличение энтропии системы возможно и без теплообмена при условии протекания неравновесного процесса. Например, представим себе, что в изолированной системе оказался механизм, включающий скрученную ( заведенную) пружину и приспособление, освобождающее ее в заранее запрограммированный момент. Однако при простом освобождении пружина неравновесно раскручивается, не совершая никакой работы. В таком неравновесном процессе также увеличивается неупорядоченность молекулярного состояния системы и возрастает ее энтропия, но уже в отсутствие поглощения теплоты извне. [7]
Если необратимые процессы вызывают увеличение энтропии системы, а при обратимых она остается постоянной, то возникает вопрос: могут ли в изолированной системе происходить процессы, приводящие к уменьшению ее энтропии. Этот вопрос, как будет показано ниже, очень важный. Однако современной науке неизвестны процессы, результатом которых явилось бы уменьшение энтропии изолированной системы. [8]
Если необратимые процессы вызывают увеличение энтропии системы, а при обратимых она остается постоянной, то возникает вопрос: могут ли в изолированной системе происходить процессы, приводящие к уменьшению ее энтропии. Этот вопрос, как будет показано ниже, является чрезвычайно важным. Ответ на него следующий: современной науке неизвестны процессы, результатом которых явилось бы уменьшение энтропии изолированной системы. [9]
Обнаружив это свойство - увеличение энтропии системы, в которой происходят необратимые процессы, Клаузиус, немецкий физик середины XIX столетия, сделал из него неверные философские выводы, перенеся механически следствия из явлений наблюдаемых в окружающей нас природе, на всю вселенную. Энтропия вселенной по Клаузиусу должна прийти к максимуму тогда, когда температуры в ней в результате тепловых процессов сравняются, при этом прекратится течение всех процессов. [10]
Это должно привести к увеличению энтропии системы. [11]
Однако, согласно (V.2), увеличение энтропии системы возможно и без теплообмена при условии протекания неравновесного процесса. Например, представим себе, что в изолированной системе оказался механизм, включающий скрученную ( заведенную) пружину и приспособление, освобождающее ее в заранее программированный момент. [12]
Однако, согласно (5.2), увеличение энтропии системы возможно и без теплообмена при неравновесных процессах. Представим себе, например, что в изолированной системе имеется механизм, включающий скрученную ( заведенную) пружину, и приспособление, освобождающее ее в заранее программированный момент. Но просто освобожденная пружина раскручивается, не совершая никакой работы. В таком неравновесном процессе также увеличивается неупорядоченность молекулярного состояния системы и возрастает ее энтропия, но уже в отсутствие поглощения теплоты извне. [13]
Положительное значение deS / dt отвечает увеличению энтропии системы в результате обмена веществом и / или энергией с внешней средой. [14]
Таким образом, необратимый процесс сопровождается увеличением энтропии системы и потерей работы. [15]
Страницы: 1 2 3 4