Двухзарядный анион
Cтраница 1
Двухзарядный анион серы S2 настолько велик ( г 1 74 А), что он легко поляризуется катионами с образованием ковалентной связи, особенно если сами катионы легко деформируются. Образованию ковалентной связи благоприятствует низкая энергия вакантных За. Поэтому для металлов с d - элек-тронами наблюдается значительное расщепление энергетических уровней, образованных d - орбиталями, что приводит к интенсивной окраске большинства сульфидов. При одинаковом электронном строении ионов окраска углубляется с увеличением их ионного радиуса. Например, различие в окраске сульфидов цинка и кадмия обусловлено большим радиусом кадмия. [1]
Двухзарядные анионы гексацианоферрата не вызывают коагуляцию белка, поскольку они имеют с ним одноименный заряд. При подкислении раствора макромолекулы белка приобретают положительный заряд. Поэтому они коагулируют от прибавления двухзарядных анионов гексацианоферрата. [2]
Для двухзарядных анионов приводится значение теплот присоединения одного протона. [3]
Для двухзарядных анионов приводятся значения теплот присоединения одного протона. [4]
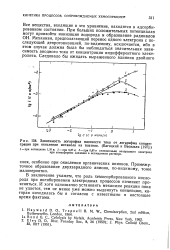 |
Зависимость логарифма плотности тока от логарифма концентрации при окислении метанола на платине. ( Багоцкий и Васильев. [5] |
Промежуточное образование двухзарядного аниона, по-видимому, тоже маловероятно. [6]
Считая, что двухзарядный анион пенталена должен относиться к аниону циклопентадиенила так же, как нафталин к бензолу, Кац ( 1962) предпринял синтез этого дианиона в качестве перспективного подхода к ранее неизвестным соединениям пенталенового ряда. [7]
Высокая реакционная способность двухзарядного аниона в значительной мере подтверждает мономолекулярный механизм. [8]
Соли красителей с двухзарядными анионами экстрагируются в десятки и сотни раз хуже, чем с однозарядными. [9]
При сравнении одно - и двухзарядных анионов в качестве возможных катализаторов реакций электронного перехода следует учитывать как различие их стандартных энтропии, так и различие их зарядов. [10]
У гексафтороком-плексов, очевидно, энергия решетки только двухзарядного аниона достаточно велика, что приводит к образованию исключительно устойчивых соединений с необычными степенями окисления. [11]
Таким образом, в растворе слабой двухосновной кислоты концентрация двухзарядного аниона ( полученного от диссоциации кислоты по второй ступени) равна второй константе диссоциации кислоты. [12]
Именно в этом, а не в больших размерах двухзарядного аниона 02 - заключается исключительно важная роль кислорода в стеклах и силикатах. [13]
Таким образом, в растворе слабой двухосновной кислоты концентрация двухзарядного аниона ( полученного от диссоциации по второй ступени) равна второй константе диссоциации. [14]
Амфотерен: рКа для БПК и его одно - и двухзарядного аниона соотв. [15]
Страницы: 1 2 3 4