Органический анион
Cтраница 1
Органические анионы могут образовывать с неорганическими катионами соли, растворимые в органических растворителях, особенно анионы кислот с большой длиной цепи атомов в молекуле: анион перфтороктановой кислоты, алкилсульфат-ионы, алкилсуль-фонат-ионы. [1]
Органический анион можно представить себе как продукт присоединения электрона к свободному радикалу и назвать, заменив слово радикал на анион. Если ион является составной частью ионного соединения, то используют суффукс ид. [2]
Органические анионы и катионы соединяются с белком при помощи такого же типа электровалентной связи. Определенные методические преимущества представляет изучение соединения белков с окрашенными ионами. Если соединение с неокрашенными ионами может быть исследовано лишь при помощи очень трудоемких аналитических методов, то соединение белков с красителями можно изучать спектроскопически, так как процесс связывания ионов красителя сопровождается изменением окраски и спектра поглощения. [3]
Органические анионы могут присоединяться к поверхности кремнезема посредством катионов металлов. [4]
Органические анионы, например анионы алкилсульфокислот предельного ряда, при адсорбции на электроде увеличивают отрицательное значение - потенциала, что приводит к ингибированию реакции восстановления анионов первой группы. В соответствии с уравнением (5.46) органические анионы ускоряют реакцию окисления европия, что указывает на электростатический характер их действия. [5]
Органические анионы могут образовывать с неорганическими катионами соли, растворимые в органических растворителях, особенно анионы кислот с большой длиной цепи атомов в молекуле: анион перфтороктановой кислоты, алкилсульфат-ионы, алкилсульфонат-ионы. [6]
Устойчивым органическим анионом, относящимся к небензоид-ным ароматическим соединениям, является анион циклопентадиени-лия ( стр. [7]
Перевод органического аниона из одной соли в другие путем непосредственного ионообмена производится с помощью катионита, если сродство к нему катиона исходной соли выше, чем катиона получаемой, или с помощью анионита - при обратном соотношении. Этот прием целесообразен, если свободная кислота неустойчива или труднорастворима; в общем случае проще выделить кислоту и затем нейтрализовать ее соответствующими основаниями. [8]
Большинство других органических анионов ( карбанионов) относятся к типу сильных оснований, и поэтому нацело протонированы даже в разбавленной кислоте. Однако протонизацию очень сильных оснований ( или, другими словами, отщепление протона от очень слабых кислот) можно использовать для определения меры основности сильно основных сред, к которым относятся не только концентрированные водные растворы щелочей, но и очень разбавленные ( 0 001 М) растворы гидроксида тетраметиламмония ( CH3) 4N OH - в смесях ДМ СО с водой различного состава. [9]
Схема ют органические анионы, вероятно, анионы клеточной мембраны аминокислот. Опытами с изотопом калия обнаружена способность внутриклеточных ионов К к практически полному обмену. Разность потенциалов на клеточной мембране зависит от разности концентраций ионов во внутренней части клетки и в окружающей ее среде, а также от проницаемости мембраны. [10]
При адсорбции органического аниона было замечено, что поверхность на границе, например, с воздухом, заряжается отрицательно. Заряд может получиться и при адсорбции дипольных молекул неэлектролитов. Благодаря этому, поверхностный слой может иметь различный заряд, в зависимости от концентрации растворов органических кислот и их солей. [11]
Основные функции органических анионов обсуждаются в разд. Кислотные центры катионов могут быть жесткими, способными образовать водородную связь б - Н, N - Н ( разд. [12]
Инд - обозначает органический анион слабой кислоты. [13]
Описан способ определения неорганических и органических анионов с помощью выпускаемой промышленностью хроматографической системы с кондуктометри-ческим детектированием. Патентованная система состоит из двух последовательно установленных колонок. Разделение осуществляется на поверхностно-пористой анионообменной смоле в среде основного элюента. Вторая колонка служит для обмена катионов в элюенте и образце на водород. Реакции обмена приводят к снижению электропроводности элюента и увеличению анионной проводимости анализируемого образца. [14]
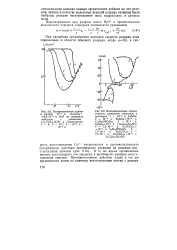 |
Поляризационные кривые в системе 10 - 3 н. Na2S2Og.| Поляризационные кривые ртутного капельного электрода в. [15] |
Страницы: 1 2 3 4