Cl-ион
Cтраница 3
Невидимому, при ПО ата вынос Cl-иона с паром связан только или почти исключительно с капельным уносом. Однако при давлении 185 ата, хотя и имеется в отличие от кремнекислоты зависимость коэффициента выноса Cl-иона от нагрузки зеркала испарения, но она несравненно слабее, чем для всех остальных примесей. [31]
При возрастании рН имеет место обратная зависимость. Мы видим, что при различных рН не только не соблюдается эквивалентность обмена ( в этом случае кривые адсорбции S042 - и вытеснения Cl-ионов должны были бы налагаться), но адсорбция S042 - и вытеснение С1 - изменяются в обратном направлении. Во всей области рН эквивалентность соблюдается лишь в точке пересечения кривых. [32]
Трубки заполнялись образцами глинистых пород и илов с естественной нлаж-ностыо и ненарушенной структурой. По истечении определенного времени образцы послойно анализировались на содержание Cl-иона и по формуле (2.91) определялся коэффициент диффузии соли. [33]
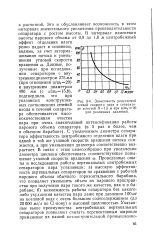 |
Зависимость допустимой осевой скорости пара в сепараторе высотой Я1 5 м при и / шс 20 для различных давлений. [34] |
С увеличением диаметра сепаратора эффективность центробежного отделения влаги при одной и той же угловой скорости вращения потока снижается, а при уменьшении диаметра соответственно возрастает. В связи с этим целесообразно при увеличении диаметра циклона обеспечивать соответствующее повышение угловой скорости вращения чв. Проведенные опыты и исследования работы вертикальных центробежных сепараторов пара установили: а) высокую эффективность вертикальных сепараторов по сравнению с работой парового объема обычного горизонтального барабана, что позволяет уменьшить объем их парового пространства при получении пара такого же качества, как и в барабане; б) возможность работы сепаратора без какого-либо ухудшения качества пара даже при давлении 100 от на котловой воде с очень большим солесодержанием ( до 20000 мг / л по Cl-иону) и высокой щелочностью. [35]
Как было показано Паркером10, в диполярных апротонных растворителях ( таких, как ДМФ, диметилсульфоксид и др.) вследствие сильной сольватации катиона галоидные ионы являются как сильными основаниями, так и сильными нуклеофильными агентами. Дигалоидный ион НХ - устойчив в ДМФ1 1 и замедляет реакцию обратного присоединения протона к образовавшемуся олефину. Основность и нуклеофильность С1 - иона в ДМФ, образующегося по приведенной реакции, является, по всей вероятности, причиной наблюдаемого каталитического действия солянокислого ДМА. Это подтверждается тем, что ряд хлоридов, диссоциирующих в ДМФ с образованием Cl-иона, также ускоряют дегидрохлорирование ПВХ. С другой стороны15, соли этих металлов практически не диссоциируют в ДМФ, тем самым исключается каталитическое действие С1 - иона. [36]
К Ю мл раствора нитрата бериллия, содержащего 7 - 22 мг Be, добавляют 5 капель индикатора Веселова и 50 мл 2 5 % - ного раствора NaF. Раствор разбавляют водой до 300 мл, добавляют 4 г борной кислоты и перемешивают до полного ее растворения. Прибавляют разбавленный раствор соляной кислоты до перехода окраски из зеленой в фиолетовую. Нагревают раствор до кипения и прибавляют к нему при перемешивании 15 мл горячего раствора ВаСЬ - Покрытый часовым стеклом стакан с осадком оставляют в кипящей водяной бане при периодическом перемешивании в течение 1 - 2 час. После коагуляции осадок отфильтровывают через стеклянный фильтр № 4 и промывают 8 - 10 раз горячей водой ( по 4 мл) до отрицательной реакции на Cl-ион и затем этиловым спиртом. Осадок BaBeF4 высушивают при ПО - 120 С. [37]
К Ю мл раствора нитрата бериллия, содержащего 7 - 22 мг Be, добавляют 5 капель индикатора Веселова и 50 мл 2 5 % - ного раствора NaF. Раствор разбавляют водой до 300 мл, добавляют 4 г борной кислоты и перемешивают до полного ее растворения. Прибавляют разбавленный раствор соляной кислоты до перехода окраски из зеленой в фиолетовую. Покрытый часовым стеклом стакан с осадком оставляют в кипящей водяной бане при периодическом перемешивании в течение 1 - 2 час. После коагуляции осадок отфильтровывают через стеклянный фильтр № 4 и промывают 8 - 10 раз горячей водой ( по 4 мл) до отрицательной реакции на Cl-ион и затем этиловым спиртом. Осадок BaBeF4 высушивают при ПО - 120 С. [38]
Совершенно иначе ведет себя вентильный электрод, где в качестве рабочей активной поверхности применена платина. Область плотностей тока, при которых идет выделение хлора, увеличивается во много раз. На этом вентильном электроде поверхность титана также со временем пассивируется. Окисленная пленка, препятствуя прохождению тока через границу титан - - водный раствор, выключает поверхность титана из янодного процесса. Как видно из рис. 3, основная доля тока при любых его значениях затрачиваестя на процесс, происходящий на платине. Cl-иона на платине, уменьшается. Так, при плотностях тока 70 и 84 ма / см 2 ( рис. 2, кривая 3) площадки становятся несколько пологими, что говорит об уменьшении доли процесса разряда ионов хлора за счет процесса пассивации. [39]
Как показали многочисленные исследования ( Эй-чисон, Чеппел, Гадфильд, American Society for Testing Materials, National Tube Co. Неблагоприятное действие оказывает невидимому повышенное содержание S, P, Si и Мп. Добавка меди в пределах 0 2 - 1 5 % улучшает антикоррозионные качества металла, особенно при воздушной К. Наиболее опасно в коррозионном отношении присутствие в растворе солей типа КС1, К2804 и NaN03, а также присутствие Cl-ионов в связи с любым катионом. Соли типа K4Fe ( CN) e, NaaCO3, как дающие нерастворимые пленки, при некоторых концентрациях могут оказывать даже защитное-действие. Хромовые соли определенно защищают металл. Аэрация и движение раствора являются одними из - главнейших факторов усиления К. Щелочные растворы низкой концентрации в большинстве случаев неопасны, в особенности если они также содержат углекислые соли. При высокой концентрации щелочи, а также при высокой 1 и давлении наблюдается сильная интеркри-сталлитная К. Эти трещинки, сливаясь, дают уже видимые внутренние-и поверхностные трещины. [40]
Раствор переносят в электролизер, который помещают в ванну со льдом. К измерениям приступают после толо, как температура раствора понизится до 2 - 3 С. Поляризуют катодно ртутный электрод ( см. гл. V) и присоединяют его к отрицательному полюсу полярографа, ртутно-сульфатный электрод - к положительному, включают мешалку я проводят электролиз 5 мин при потенциале 0 в. Прекращают перемешивание, дают раствору успокоиться 10 - 15 сек и регистрируют катодную поляризационную кривую растворения хлорида ртути в интервале потенциалов ( 0) - ( - 1 0) в. Измеряют максимальный катодный ток, который наблюдается в области потенциалов от ( - 0 2) до ( - 0 4) в. Концентрацию Cl-ионов находят методом добавок. [41]
Страницы: 1 2 3