Восстановление - катион
Cтраница 1
Восстановление катионов из комплексонатов протекает также необратимо с некоторым уменьшением предельно диффузионных токов. Поэтому константы устойчивости по сдвигу потенциалов полуволн рассчитаны только для комплексов меди. [1]
Восстановление катиона феррициния в водных растворах протекает с автоингибирова-нием. Замена воды этанолом устраняет ингибирование, так как при этом ослабляется адсорбция продукта электродного процесса - ферроцена - на ртути. Наблюдается параллелизм между ослаблением ингибирования и ростом растворимости ферроцена в водно-этаноловых смесях. Предельный ток окисления ферроцена в интервале 60 - 100 % этанола растет в соответствии с уменьшением вязкости среды. Зависимость предельного тока восстановления катиона феррициния от состава растворителя обусловлена изменением не только вязкости среды, но и сольватацией катиона феррициния. От состава растворителя сильно зависят также величины Е12, что имеет отношение к использованию системы ферроцен - феррициний как стандарта при сопоставлении нормальных потенциалов, измеренных в разных растворителях. [2]
Если восстановление катионов сопровождается химическим перенапряжением, вычислить константу равновесия / Ср предшествующей химической стадии, воспользовавшись величиной предельного тока при определенном значении со и известной величиной толщины реакционного слоя бр. [3]
Происходит восстановление катионов пиридина ( РуН), образуются радикалы РуН, инициирующие полимеризацию. На основании ИК-спектра и элементарного анализа предложено частичное гидрирование пиридина с последующим раскрытием цикла и образованием полимера с сопряженными связями. [4]
После восстановления катиона данного сорта сила тока будет оставаться постоянной до определенного значения потенциала, при котором начнется выделение другого катиона и сила тока вновь резко возрастет. [5]
Потенциал восстановления катиона, при всех прочих условиях, зависит ркже и от концентрации катионов в растворе. [6]
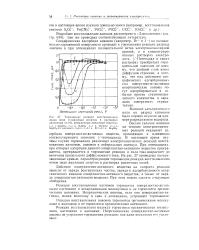 |
Торможение реакции восстановления ионов меди я-амиловым спиртом в растворах различных солей, насыщенных амиловым спиртом. [7] |
Реакции восстановления катионов тормозятся поверхностно-активными катионами и незаряженными молекулами и не тормозятся органическими анионами. Неорганические анионы, если они поверхностно-активны, меняя величину и знак / - потенциала, устраняют торможение. [8]
Легкость восстановления катионов на катоде соответствует ряду активности металлов. Чем правее в этом ряду находится металл, тем легче идет его восстановление. [9]
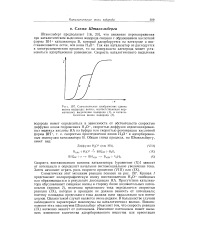 |
Схематическое изображение сдвига волны водорода. волна, соответствующая нормальному выделению водорода ( 1, и каталитическая волна водорода ( 2. [10] |
Скорость восстановления катиона катализатора [ уравнение ( X) ] зависит от потенциала и определяет начальное экспоненциальное увеличение тока. [11]
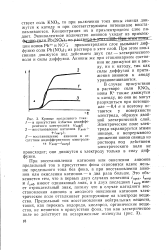 |
Кривые предельного тока. [12] |
При восстановлении катионов или окислении анионов предельный ток в присутствии фона становится вдвое меньше предельного тока без фона, а при восстановлении анионов или окислении катионов - в два раза больше. Это объясняется тем, что в первых двух случаях величины / пред, мигр и гдиф имеют одинаковый знак, а в двух последних jMlirp имеет отрицательный знак, потому что в случае катодного восстановления анионов и анодного окисления катионов электрическое поле отталкивает реагирующие на электроде вещества. [13]
При восстановлении катионов металлы образуют с ртутью амальгамы. Равновесный потенциал амальгамного электрода зависит как от концентрации катионов в растворе, так и от концентрации металла в амальгаме ( см. уравн. С увеличением силы катодного тока концентрация катионов в приэлектродном слое уменьшается, а металла в поверхностном слое в ртути - возрастает. [14]
При восстановлении катионов ( z 0) электростатическое действие поля облегчает их подход к поверхности электрода и, как следует из ( 19), знаки у А. На положительно заряженной поверхности электрода, наоборот, электростатическое действие поля замедляет электродные процессы с участием катионов и ускоряет процессы с участием анионов. [15]
Страницы: 1 2 3 4