Восстановление - молекула
Cтраница 1
Восстановление молекулы происходит в результате каталитического гидрирования над металлическими катализаторами в гетерогенных или гомогенных условиях, а также при действии разнообразных восстановителей ( разд. В случае гетерогенного процесса молекула олефина и молекула водорода адсорбируются на поверхности катализатора, что приводит к сильному ослаблению связей; в результате происходит присоединение водорода к олефину in situ, как это представлено на схеме [, стр. [1]
Восстановление молекулы азота до двух молекул аммиака требует присоединения электронов. [2]
Гальваностатическое восстановление молекул 5-бром - 2-ацетилтиофена, адсорбированных на ртути. [3]
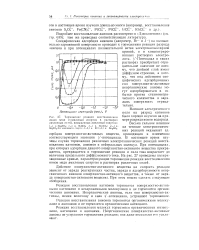 |
Торможение реакции восстановления ионов меди я-амиловым спиртом в растворах различных солей, насыщенных амиловым спиртом. [4] |
Реакции восстановления молекул тормозятся органическими молекулами, катионами и анионами. Неорганические поверхностно-активные анионы не устраняют торможения реакции; они даже несколько его усиливают. [5]
Поэтому безЬарьерпое восстановление молекул НХ ( в отличие от разряда ионов Н30) может существенно зависеть от состава электролита. [6]
Сам процесс восстановления молекулы органического вещества на ртутном капельном электроде, как можно предположить, происходит следующим образом. Этим местом обычно является атом или группа атомов с минимально возможной в данных условиях плотностью электронов. [7]
Зависимость предельных токов восстановления недвссоциирован-иых молекул ( а) и анионов ( б) 2-фенил-индандиона - 1 3 от рН при различном содержании этилового спирта в растворе ( объемн. [8]
В катодном полуэлементе электрохимический процесс восстановления молекул воды в гидроксильные ионы и биохимический процесс превращения сульфатных ионов под действием бактерий протекают одновременно. Бактерии Desulfovibrio desulforicans, восстанавливая в католите ионы сульфата в ионы сульфида по биохимическому механизму, играют роль агентов переноса электронов па поверхность катода. [9]
Это говорит о том, что восстановление молекулы n - нитродифенила в нейтральной и щелочной среде идет с присоединением 4 - х электронов до гидроксиламина, а в сильнокислой среде с присоединением 6-ти электронов до амина. [10]
Определение количества электронов, участвующих в восстановлении молекулы ыетнлметакрилата, методом полярографической кулонометрии дает величину, близкую к 2, что говорит о восстановлении молекулы с присоединением двух электронов. [11]
С наступлением темноты из-за быстрой рекомбинации ( восстановления молекул) исчезают область слоя D и уступ на уровне слоя F. В то же время электронная концентрация области Е сохраняет постоянное значение в течение всей ночи. [12]
Электрохимическая коррозия, при которой катодным процессом является восстановление молекул кислорода, называется коррозией с кислородной деполяризацией. Электрохимическая коррозия, при которой катодным процессом является восстановление ионов водорода, называется коррозией с водородной деполяризацией. [13]
Обе величины близки к 2, что характеризует процесс восстановления молекулы ацетилдифе-нила как проходящий с участием двух электронов. [14]
Предполагается, что катодные пики всех редкоземельных элементов обусловлены восстановлением молекул воды, входящих в состав комплексной частицы. Найдены коэффициенты диффузии, коэффициенты переноса, константы скорости электродных процессов. Процессы являются необратимым и осложнены предшествующими химическими реакциями. [15]
Страницы: 1 2 3 4