Амидный азот
Cтраница 3
При этом хотя бы один водород должен быть в орто-положении к амидному азоту. Общее число углеродных атомов в двух алкильных группах не должно быть более пяти. Если алкилы содержат более 5 атомов углерода, то активность соединения падает. [31]
Это объясняется тем, что увеличение кольца затрудняет мезомерное взаимодействие между амидным азотом и бензольным кольцом, тогда как мезомерное взаимодействие между NH и СО увеличивается и значение частоты приближается к частоте амида с нормальной цепью. Объясняется это вкладом крайней структуры ( 8) для свободного соединения и структуры ( 9) для соли. [32]
В сложных удобрениях азот может содержаться в виде аммонийного, нитратного или амидного азота, а чаще всего в сочетании двух форм: нитроаммофоска, диаммонитрофоска, карбоаммофоска и др. Методики определения данных форм азота различны. Для определения общего азота применим метод отгонки аммония с предварительным восстановлением нитратного азота до аммонийного, для определения аммонийного азота - объемный хлораминовый метод или гипохлоритный ( с визуальным или потенциометрическим окончанием анализа), карбамидного азота - спектрофотометриче-ский метод, нитратного азота - объемный метод. [33]
Все это свидетельствует о том, что чем больше возможность внутримолекулярного протежирования амидного азота в нуклеотидо - ( P - - N) - пептиде, тем менее устойчива нуклеотидопептидная связь в нем. [34]
Наличие заметного расщепления фосфоамидной связи в оксиэтило-вом эфире XXIII не исчерпывается внутримолекулярной протонизацией амидного азота с последующей атакой молекулой воды ( на стр. Одновременно с отщеплением протона от оксиэтильной группы происходит увеличение отрицательного заряда на гидроксильном кислороде, который вследствие этого легко атакует атом фосфора. Результатом такой атаки является перегруппировка ( путь 2), заключающаяся в разрыве фосфоамидной связи с одновременным образованием фосфо-эфирной связи. [35]
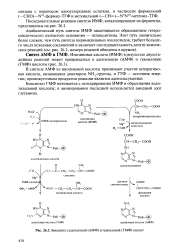 |
Биосинтез адениловой ( АМФ и гуаниловой ( ГМФ кислот. [36] |
Биосинтез ГМФ начинается с дегидрирования ИМФ и образования ксан-тидиловой кислоты; в аминировании последней используется амидный азот глутамина. [37]
Как видно из табл. 83, уже на третий год эксплуатации крупного цеха карбамида себестоимость амидного азота лишь на 6 % превышала себестоимость нитратного. При этом следует отметить, что мощность производства нитрата аммония почти в 3 раза больше мощности производства карбамида. [38]
В ходе очистки сока до выпарки почти полностью удаляются белки и аммиачный азот, 40 - 50 % амидного азота, 5 - 8 аминного азота, 40 - 45 безазотистых органических веществ, 10 - 12 % золы. [39]
У растений с кислым клеточным соком накапливается значительно больше аммиака по сравнению с амидами, а у растений с меньшей кислотностью сока амидный азот преобладает над аммиачным. [40]
Наряду с приведенными в табл. 24 соединениями гербицидными свойствами обладают и многие другие амиды и анилиды, содержащие различные заместители как при амидном азоте, так и в ароматическом радикале [94, 97, 98, 100 - 107], а также производные N-циклогексилхлор - и N-циклогексилбромацетамидов. По ареалу действия эти препараты аналогичны производным монохлоруксусной кислоты, но имеют несколько другую избирательность действия. [41]
Задача определения азота, входящего в состав амидов, содержащихся в физиологических жидкостях ( и тканях), отличается от задачи определения содержания амидного азота в молекуле белка. В физиологических жидкостях, вследствие присутствия мочевины, а также других соединений, содержащих азот, метод полного гидролиза исследуемых соединений использован быть не может. Поэтому анализируемый образец подвергают гидролизу в мягких условиях, в результате которого только амиды, входящие в состав образца, превращаются в аммиак. При анализе некоторых жидкостей, например мочи, серьезной помехой является аммиак, поскольку он присутствует в количествах, значительно превосходящих количество амидов, и определяется с помощью любого метода, который может быть использован для определения аммиака, образующегося в результате гидролиза амидов. [42]
В то же самое время, при образовании связи между сериновым кислородом и карбонильным углеродом, происходит ослабление связи между карбонильным углеродом и амидным азотом, и этому ослаблению способствует наличие поблизости атома водорода, ранее принадлежавшего сери-ну, а теперь связанного с азотом гистидина. Половина цепи субстрата теперь отщепляется, а другая половина остается присоединенной к сериновой боковой цепи фермента. Конфигурация связей вокруг карбонильного атома углерода снова становится плоской тригональной и среди них снова имеется двойная связь СО. [43]
При изучении такого экстракта было установлено, что на каждый 1 моль меченого гипоксантина, синтезированного из С14 - глицина, используются 2 моль амидного азота глутамина и 1 моль азота либо глутаминовой, либо аспарагиновой кислоты. Чтобы выяснить, какая из этих аминокислот служит предшественником N-1, измеряли количество образовавшегося С14 - гипоксантина после инкубации ферментного препарата из печени голубя с С14 - глицином, С02, формиатом, рибозо-5 - фосфа-том и АТФ. При добавлении глутамина, аспарагиновой или глутаминовой кислоты выход пурина увеличивался. [44]
Ван-Слайк и его сотрудники [65] в опытах на собаках с выведенными под кожу почками показали, что большая часть аммиака мочи образуется за счет амидного азота глутамина. Эти авторы параллельно определяли концентрацию глутамина в крови почечных сосудов и образование аммиака мочи. [45]
Страницы: 1 2 3 4