Квантовая ячейка
Cтраница 3
Ниже приведено распределение электронов по квантовым ячейкам в некоторых октаэдрических комплексах в слабом и сильном полях. В тех случаях, когда число электронов в ионе комплексо-образователя больше, чем число орбиталей с низкой энергие имеют место различия. Эте связано с тем, что в случае слабого поля РД и электроны в квантовых ячейках распределяются в соответствии с правилом Гунда. Ион металла находится в состоянии с высоким спином. В случае сильного поля в пределах подуровня при распределении электронов соблюдается правило Гунда. [31]
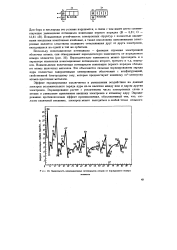 |
Зависимость ионизационных потенциалов атомов от порядкового номера. [32] |
Повышенная устойчивость электронных структур с полностью вакантными внешними квантовыми ячейками, а также наполовину заполненными электронами является следствием взаимного отталкивания друг от друга электронов, находящихся на одной и той же орбитали. [33]
Таким образом, распределяя электроны по квантовым ячейкам, можно выявлять число неспаренных электронов в атоме. [34]
Таким образом, размещая электроны по квантовым ячейкам, можно выявить число неспаренных электронов в атоме. [35]
Таким образом, распределяя электроны по квантовым ячейкам, можно выявить число неспаренных электронов в атоме. [36]
Таким образом, распределяя электроны по квантовым ячейкам, можно выявлять число неспаренных электронов в атоме. [37]
Таким образом, размещая электроны по квантовым ячейкам, можно выявить число неспаренных электронов в атоме. [38]
Как распределятся электроны в этом атоме по квантовым ячейкам. [39]
Структуру электронных оболочек изображают с помощью энергетических или квантовых ячеек. Каждая ячейка обозначается клеткой. [40]
Более полно описывает состояние электронов в атомах метод квантовых ячеек, использующий все четыре квантовых числа. Каждой ячейке отвечает определенная орбиталь, электрон изображается в виде стрелки, а направление последней олицетворяет спиновое квантовое число. Свободная ячейка означает свободную орбиталь, которую может занимать электрон при возбуждении атома. [41]
Очень часто структуру электронных оболочек изображают с помощью квантовых ячеек - это так называемые графические электронные формулы или схемы. Каждая такая ячейка обозначается клеткой: клетка - орбиталь, стрелка - электрон, направление стрелки - направление спина, свободная клетка - свободная орбиталь, которую может занимать электрон при возбуждении. [42]
В элементах VA, VIA и VILA подгрупп свободных квантовых ячеек уже не остается и начинается спари-электронов сначала в S -, а затем и в / - ячейках. [43]
Два электрона с противоположными спинами, занимающие одну квантовую ячейку, называют спаренными. Пользуясь этой терминологией, можно сказать, что, согласно теории Гейтлера и Лондона, водород способен к образованию молекулы Н2 потому, что в его атоме имеется один неспаренный электрон, а гелий не может образовать молекулу Не2 ввиду того, что оба электрона в атоме Не являются спаренными. [44]
Два электрона с противоположными спинами, занимающие одну квантовую ячейку, называют спаренными. Пользуясь этой терминологией, можно сказать, что согласно теории Гейтлера и Лондона водород способен к образованию молекулы Н2 потому, что в его атоме имеется один неспаренный электрон, а гелий не может образовать молекулу Не2 ввиду того, что оба электрона в атоме Не являются спаренными. [45]
Страницы: 1 2 3 4