Аквакатион
Cтраница 1
Аквакатионы [ Э ( Н2О) 6 ] ( Э - Fe, Со, Ni) и [ Fe ( H2O) B ]: 1 являются слабыми кислотами в водном растворе. [1]
Аквакатионы [ М ( Н2О) ] 3 содержат во внутренней сфере более шести молекул воды, например [ Nd ( H20) e ] 3J Склонность их к гидролизу растет от лантана к лютецию параллельно уменьшению радиуса ионов, причем радиусы гидратированных ионов в этом же ряду увеличиваются. [2]
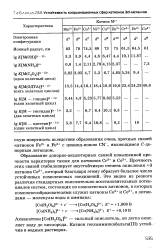 |
Устойчивость координационных сфер катионов Зс / - металлов. [3] |
Аквакатион [ Со ( Н20) 6 ] 3 - сильный окислитель, он легко окисляет воду до кислорода. Катион гексамминкобальта ( Ш) устойчив в водных растворах. [4]
Аквакатион [ Мп ( Н2О) 6 ] 3 в водных растворах неустойчив. [5]
Аквакатион [ Со ( Н2О) 6 ] 3 - настолько сильный окислитель, что он окисляет воду. Более устойчивы комплексные соединения Со3 с другими лигандами, например молекулами аммиака. [6]
Аквакатионы ванадия ( II) и ( 111) проявляют сильные восстановительные свойства. Оба эти катиона окисляются кислородом воздуха, а ион V ( H2O) 6 ] 21 - даже водой с выделением водорода. [7]
Аквакатионы металлов, имеющих степень окисления ( III), - еще более активные доноры протонов. [8]
Одноядерные аквакатионы висмут не образует. [9]
Аквакатион олова ( П) проявляет сильные кислотные свойства и поэтому устойчив только при рН 1 в среде хлорной или азотной кислот, анионы которых не обладают заметной склонностью входить в состав комплексов олова ( П) в качестве лигандов. При разбавлении таких растворов выпадают осадки основных солей различного состава. Большинство солей свинца ( П) ( например, иодид, хлорид, сульфат, хромат, карбонат, сульфид) малорастворимы в воде. [10]
Аквакатионы алюминия, галлия и индия в водном растворе подвергаются протолизу и проявляют функции слабых кислот. [11]
Аквакатионы лантаноидов, кроме Се, Gd и Yb, придают водным растворам ту или иную окраску. [12]
Аквакатионы цинка ( П) и кадмия ( П) в растворе являются протолитами со свойствами слабых кислот. Сульфиды ZnS и CdS малорастворимы в воде; при кипячении их с концентрированной азотной кислотой образуются растворимые сульфаты. [13]
 |
Физико-химические свойства хрома, молибдена и вольфрама. [14] |
Образующийся аквакатион хрома ( II) придает раствору ярко-голубую окраску. [15]
Страницы: 1 2 3 4