Разряженный аккумулятор
Cтраница 1
Разряженный аккумулятор необходимо поставить на зарядку. Ток заряда не должен превышать 12 ма. Лучше всего всегда заряжать аккумулятор именно таким током в течение 15 час. Если заряжать аккумулятор током, превышающим это значение, то выделяющиеся газы не будут успевать своевременно поглощаться электродами, в результате один или несколько элементов аккумулятора могут вспучиться под давлением скопившихся газов и будет нарушена герметичность. [1]
Если разряженный аккумулятор оставить на некоторое время в бездействии, то напряжение его снова восстанавливается до своей средней величины 2 в. Это явление носит название отдыха аккумулятора. [3]
У разряженного аккумулятора напряжение на зажимах каждого элемента вместо 2 в падает до 1 8 в. Дальнейшее разряжение аккумулятора разрушает пластины. [4]
У разряженного аккумулятора активная масса положительных пластин состоит из гидрата закиси никеля Ni ( OH) 2 с примесью чешуйчатого графита. [5]
В пластинах разряженных аккумуляторов как результат химических реакций при разряде содержится значительное количество сульфата. Однако этот сульфат, как уже указывалось выше, состоит из мелких кристаллов и при заряде легко превращается в двуокись свинца и губчатый свинец. [6]
При подключении разряженного аккумулятора к внешнему источнику тока ( зарядка) электрохимические процессы полностью обращаются. [7]
Напряжение на зажимах разряженного аккумулятора в процессе зарядки вначале быстро растет, поэтому следует отмечать показания электроизмерительных приборов через каждые 20 - 30 сек, а затем через каждые 10 - 15 мин. [8]
При дальнейшем хранении разряженного аккумулятора в нем возникает нежелательный процесс сульфатации пластин, приводящий к постепенному уменьшению напряжения и, наконец, порче аккумулятора. Сульфатация пластин выражается сначала в появлении на электродах отдельных белых пятен, которые затем в течение нескольких недель превращаются в белую корку, состоящую из сернокислого свинца. [9]
При длительном хранении разряженного аккумулятора на поверхности и в порах активной массы положительных и отрицательных пластин образуется сплошной слой крупных кристаллов PbSO4, который как бы изолирует активную массу пластин от электролита и, закупоривая поры активной массы, препятствует проникновению электролита в глубь пластин. Крупные кристаллы PbSO4 трудно растворяются в электролите. [10]
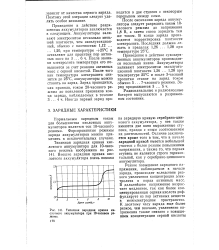 |
Типичная зарядная кривая кислотного аккумулятора при 10-часовом ре. [11] |
Приведение в действие разряженных аккумуляторов заключается в следующем. После заливки электролита температура его повышается за счет реакции активных масс с серной кислотой. [12]
При постановке на заряд частично разряженных аккумуляторов длительность заряда должна быть уменьшена так, чтобы при заряде емкость не превышала более 120 - 150 % снятой на предыдущем разряде во избежание порчи аккумуляторов. Аккумуляторы ЦНК-09 обеспечивают отдачу гарантированной емкости в случае их эксплуатации при положительных температурах. Понижение температуры до нуля заметно сказывается на значении среднего разрядного напряжения и емкости, отдаваемой аккумуляторами при разряде до 1 В. Разрядные кривые при различной температуре показаны на рис. 5.4. При температуре 10 С аккумуляторы отдают в среднем около 50 - 60 % фактической емкости. [13]
 |
Схематическое изображение основных окислительно-восстановительных процессов, протекающих в свинцовом аккумуляторе. [14] |
Анализ состава электродных масс заряженного и разряженного аккумулятора, а также данные опытов по определению изменения концентрации серной кислоты при заряде и разряде подтверждают ТДС, но наиболее важным доказательством достоверности ТДС является термодинамическое ее обоснование, которое может быть выполнено несколькими путями. [15]
Страницы: 1 2 3 4
