Активация - диффузия
Cтраница 2
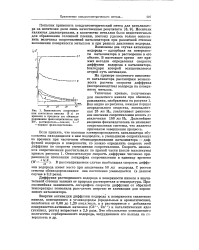 |
Зависимость сопротивлэ - ная 25 мл Ш, увеличивает равновес-ния скелетного никеля ( 3 г от значение сопротивления вплоть до. [16] |
Энергия активации диффузии водорода к поверхности скелетного никеля, помещенного в углеводороды ( предельные и ароматические), колеблется от 0 60 до 1 20 ккал / молъ, а в растворителе с добавками поверхностно-активных катионов ( Cd, Zn) и каталитических ядов ( унитиол, ртуть) возрастает в 2 5 раза. [17]
Энергия активации диффузии Q обычно всегда ниже, чем энергия активации химической реакции А, и при высоких температурах наиболее вероятен диффузионный режим. [19]
Энергия активации диффузии азота в гафнни при образовании твердых растворов в интервале 1149 - 1307 К равна Е 238 кДж / моль. [20]
Энергия активации диффузии азота в ниобии, определенная [28] при помощи высокочастотного внутреннего трения при более высоких температурах - от 285 до 583 С и равная 35720 кал / г-атом, хорошо согласуется с приведенными выше результатами. [21]
Энергия активации диффузии кобальта в молибдене по этим данным, по-видимому, сильно занижена. [22]
Энергия активации диффузии ED складывается из энергии, требуемой для образования дырок против сил когезии среды, и энергии, необходимой для действительного переноса молекулы через окружающую структуру. Энергия активации диффузии молекул в жидкостях низкого молекулярного веса составляет величину порядка 5 - 10 ккал / моль, в то время как диффузия Б полимерных веществах обычно характеризуется более высокими значениями энергии активации. [23]
Энергия активации диффузии ED представляет собой энергию, необходимую для прохождения одного моля газа в элементарном акте диффузии. Ее, вероятно, можно рассматривать как работу разделения цепей, в связи с чем значение ED увеличивается с ростом размеров молекул газа. [24]
Энергия активации диффузии ионов в ионите, как правило, превышает энергию активации диффузии в воде и в растворах и приближается к ним лишь в слабо сшитых легко набухающих ионитах при диффузии ионов, не образующих с функциональными группами локализованных структур. Обычная ее величина составляет 6 - 8 ккал / моль, однако в некоторых конкретных случаях ( диффузия крупных органических ионов в сильно сшитых ионитах, диффузия некоторых ионов в цеолитах и некоторых неорганических ионитах) она может достигать 20 - 30 и даже 60 - 80 ккал / моль. [25]
Энергия активации диффузии водорода для образцов со структурой аустенита на основании этих данных получилась равной - 8600 кал / моль. [26]
Энергия активации диффузии Q характеризует энергию связи атомов в кристаллической решетке. [27]
Энергия активации диффузии ED складывается из энергии, требуемой для образования дырок против сил когезии среды, и энергии, необходимой для действительного переноса молекулы через окружающую структуру. Энергия активации диффузии молекул в жидкостях низкого молекулярного веса составляет величину порядка 5 - 10 ккал / моль, в то время как диффузия в полимерных веществах обычно характеризуется более высокими значениями энергии активации. [28]
Энергия активации диффузии Q обеспечивает переход атомов из одного положения в решетке в другое. Необходимый для такого перехода избыток энергии приобретается атомом от его соседей благодаря тому, что атомы непрерывно обмениваются кинетической энергией. Так как величина энергии активации входит в показатель степени, то она очень сильно влияет на величину коэффициента диффузии. [29]
 |
Температурные зависимости второго момента спектров ПМР бензола, адсорбированного цеолитами СаХ и NaX. [30] |
Страницы: 1 2 3 4