Активация - кислород
Cтраница 3
Некоторые побочные продукты ксантогенирования ( например, Na2S) могут ускорять окислительную деструкцию вследствие активации кислорода; другие ( например, Na2S2) - задерживать деструкцию. [31]
Казалось бы, что при значительных катодных смещениях потенциалов катализатора лимитирующей стадией реакции должна быть активация кислорода и скорость реакции будет понижаться с увеличением концентрации спирта. [32]
Однако опыты, описанные в [511], не доказывают, что в реальных условиях катализа окисления H2S на глиноземе активация кислорода играет решающую роль. На 7 - А12О3, не подвергнутом описанной специальной окислительной обработке, сероводород при комнатной температуре кислородом воздуха не окисляется. [33]
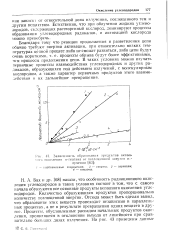 |
Зависимость образования продуктов непол. [34] |
Естественно, что при облучении жидких углеводородов, содержащих растворенный кислород, доминируют процессы образования углеводородных радикалов, и активацией кислорода можно пренебречь. [35]
При окислении же более устойчивой молекулы - SOa наряду с ее активацией при координационном связывании с V2O5, имеющей кислотный характер, существенное значение приобретает и активация кислорода. [36]
Большие перспективы МНА связаны с использованием импульсного генератора нейтронов для активации пород, поскольку это позволит определять содержание изотопов с Тчг в несколько секунд, в частности 16N, являющегося продуктом активации кислорода. Регистрация наведенной активности кислорода расширяет возможности метода при установлении ВНК, выделении угольных пластов, залежей серы и решении ряда других задач. [37]
Схема раздельной активации кислорода и углеводорода позволяет в ряде случаев удовлетворительно объяснить возможность прртекания реакции окисления углеводородов, однако в последнее время все большую значимость приобретают теоретические предпосылки и экспериментальные данные в пользу активации кислорода и углеводорода на одном реакционном центре иона металла переменной валентности, способном образовать комплексные соединения. [38]
С другой стороны, очевидно, что катализаторы окисления неорганических соединений должны иметь и свойства, общие с контактами окисления органических веществ, поскольку в обоих случаях, как правило, необходимым этапом реакции является активация кислорода. [39]
Схема раздельной активации кислорода и углеводорода хотя и позволяет в ряде случаев объяснить протекание реакции окисления углеводородов, однако за последнее время все большую значимость приобретают теоретические предпосылки, подтвержденные экспериментальными данными, в пользу активации кислорода и углеводорода на одном центре, которым является катализатор - металл переменной валентности, способный образовывать комплексные соединения. По отношению к атому металла кислород является акцептором, а молекула RH - донором. [40]
Тот факт, что тирозиназа является смесью амипоацидазы и фенолазы, подтверждает далее высказанное несколько лот тому назад Матюзом21 предположение, что ферменты, которые до сих пор называли оксидазами, охватывают два класса ферментов: один из них обусловливает активацию кислорода, а другой, значительно более важный, вызывает расщепление субстратов на различные молекулы, обладающие восстановительными свойствами. Ферменты второго рода рассматриваются Матюзом скорее как восстановительные ферменты, и он приписывает им определенную специфичность, в то время как сами оксидазы никакой специфичностью не обладают. [41]
В результате образования промежуточного комплекса катализатора с НС1 не только ослабляются связи Н - С1 и Me - С1 ( в случае хлоридного контакта), но и понижается степень ионности катионов переходного металла, что, как отмечает Борес-ков [248], способствует активации кислорода. Именно поэтому, очевидно, соединения переходных металлов значительно активнее соединений непереходных. [42]
Гидратация анионов ОН - дает дополнительную энергию, возбуждающую молекулы кислорода. Активация кислорода происходит и при добавлении к кислороду некоторых способных флуоресцировать красителей. Возможно, что часть энергии, обычно испускаемая красителем при флуоресценции, поглощается кислородом и активирует его. Весьма вероятно, что окислительно-восстановительные процессы в биологических истемах протекают как раз через стадию образования свободных радикалов. [43]
Механизм этого окисления был разработан А. Н. Бахом еще в начале 1897 г. в его труде О роли перекисей в процессах медленного окисления. Энергия, необходимая для активации кислорода в процессе медленного окисления, не получается извне, а доставляется самим окисляемым веществом. Поэтому при обычных температурных условиях молекулярным кислородом могут окисляться лишь химически ненасыщенные, аутоксидабель-ные вещества, тогда как насыщенные остаются без изменения. Аутоксида-бельные вещества, приходя в соприкосновение с кислородом, не расщепляют его молекулу на свободные атомы ( как это думали раньше), а превращают эту молекулу в радикал, где только одна связь является разорванной. Указанный радикал и присоединяется к окисляемому веществу. При этом неизбежно должны образовываться перекиси, которые, являясь весьма неустойчивыми и химически активными веществами, способствуют дальнейшему окислению. [44]
Классическими работами академика А. Н. Баха создана перекисная теория медленного окисления. Согласно этой теории энергия, необходимая для активации кислорода, проводящего процесс спонтанного окисления, получается от химически ненасыщенных соединений, вступающих с ним во взаимодействие. [45]
Страницы: 1 2 3 4