Активация - молекула
Cтраница 1
Активация молекул в газовой фазе, необходимая для преодоления потенциального барьера в ходе химической реакции, вызывается столкновениями молекул. В случае мономолекулярной реакции столкновения с другими частицами играют лишь роль поставщика энергии. При столкновении энергия поступательного движения частично переходит в колебательное движение ядер в молекуле, причем этот процесс сопровождается сложным обменом энергии между различными колебательными степенями свободы. [1]
Активация молекул может быть вызвана не только повышением температуры, но и с помощью лучистой энергии. [2]
Активация молекул достигается повышением температуры, поглощением лучистой энергии, воздействием электрического поля с определенной длиной волны, радиацией, каталитическим воздействием. [3]
Активация молекул, кроме соударений, может быть вызвана и другими внешними причинами, например действием лучистой энергии, электрического разряда, ударами электронов, а-частиц и нейтронов радиоактивного излучения. [4]
Активация молекул посредством чисто конфигурационных изменений, вызываемых какими-то факторами, действующими в надлежащий момент, расширяет перспективы использования этих характерных веществ в образовании биологических систем. [5]
Активация молекул в мономолекулярных реакциях происходит за счет столкновений реагирующих молекул друг с другом. [6]
Активация молекул А происходит в результате бимолекулярных столкновений, активные молекулы А, с одной стороны, дезактивируются в бимолекулярных столкновениях, с другой - подвергаются превращению, например распадаются. [7]
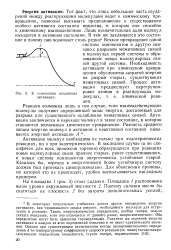 |
К пояснению механизма Ровке атомов в реагирующих мо-активации. лекулах, т. е. химической реак. [8] |
Активация молекул необходима не только при эндотермических реакциях, но и при экзотермических. В последнем случае ( а он специфичен для всех процессов горения) образующиеся при реакциях новые молекулярные связи прочнее старых, ранее существовавших, и новая система компонентов энергетически устойчивее старой. Казалось бы, переход в энергетически более устойчивую систему должен был протекать самопроизвольно. Для объяснения причины, по которой это не происходит, удобно воспользоваться наглядным примером. [9]
Активация молекул может происходить по / г действием различного рода энергии. Так, молекулы некоторых веществ активируются под действием химической энергии, других-под действием световой, но молекулы наибольшего числа веществ активируются под действием теплояой энергии. [10]
Активация молекул реагента может осуществляться или путем координации, или путем присоединения. В рассмотренном каталитическом цикле гидрирования ( схема 27.3) молекула водорода активируется путем присоединения к металлу, тогда как молекула алкена путем координации. [11]
При активации молекул N2 ( нагреванием, действием электроразряда или ионизирующих излучений) азот) бычно выступает как окислитель и лишь при взаимодействии с фтором и кислородом - как восстановитель. [12]
Если активация молекул в обоих типах реакций происходит в результате соударений, то при мономолекулярной реакции последнее соударение, в котором молекула приобретает нужный для распада минимум энергии, отделено от самого акта распада некоторым отрезком времени; в бимолекулярной реакции момент реакции совпадает с - моментом последнего соударения. [13]
Если активация молекул в обоих типах реакций происходит в результате соударений, то при мономолекулярной реакции последнее соударение, в котором молекула Приобретает нужный для распада минимум энергии, отделено от самого акта распада некоторым отрезком времени; в бимолекулярной реакции момент реакции совпадав с моментом последнего соударения. [14]
При активации молекул N2 ( нагреванием, действием электроразряда или ионизирующих излучений) азот обычно выступает как окислитель и лишь при взаимодействии с фтором и кислородом - как восстановитель. [15]
Страницы: 1 2 3 4