Активация - молекулярный водород
Cтраница 2
Помимо транспорта электронов в мембранах Fe-S - белки участвуют в фиксации молекулярного азота, в восстановлении сульфита и нитрита, в фотосинтезе, в освобождении и активации молекулярного водорода и в окислении алка-нов. Некоторые железосерные белки получили название по своему происхождению или по функции: ферредок-син, путидаредоксин, рубредоксин, адренодоксин. [17]
Использование растворителей, обладающих донорными свойствами, а также незначительных количеств молекулярного водорода приводит к частичной стабилизации образующихся при крекинге продуктов, что и объясняет образование в условиях этого процесса в основном высокомолекулярных продуктов, Высокая концентрация молекулярного водорода и наличие катализаторов, способствующих повышению глубины расщепления угольных компонентов, их стабилизации за счет активации молекулярного водорода, а также наличие растворителя, являющегося донором водорода ( условия процесса гидрогенизации), приводит к значительному повышению степени конверсии и выходу продуктов реакции с более низкомолекулярной массой. [18]
Гомогенное гидрирование алкенов молекулярным водородом при участии комплексных металлоорганических катализаторов - соединений переходных металлов типа МХЛ ( где М - Ni, Co, Си, Fe; п - 2 3; X - галоген) с металлоорганическими восстановите-лями ( Алк. Процесс состоит из: 1) активации молекулярного водорода, заключающейся в разрыве связи Н - Н в результате его взаимодействия с металлоорганическим соединением и образования гидридного комплекса; 2) непосредственного гидрирования, при котором гидридный комплекс присоединяется к алкену и образует связь металл - углерод; гидрогенолиз этой связи приводит к конечному продукту и гидриду переходного металла, снова включающемуся в реакцию. [19]
Гомогенное гидрирование алкенов молекулярным водородом при участии комплексных металлоорганических катализаторов - соединений переходных металлов типа МХП ( где М - Ni, Co, Cu, Fe; п - 2 3; X - галоген) с металлоорганическими восстановителями ( Алк) 3А1, ( CH3CH2O) jB - приобретает практическое значение вследствие мягких условий процесса ( 30 - 50 С и 3 - Ю5 - 5 - Ю5 Па), легкости регенерации катализатора и высокой эффективности реакции вследствие того, что катализатор и гидрируемое соединение находятся в растворе. Процесс состоит из: 1) активации молекулярного водорода, заключающейся в разрыве связи Н - Н в результате его взаимодействия с металлоорганическим соединением и образования гидридного комплекса; 2) непосредственного гидрирования, при котором гидридный комплекс присоединяется к алкену и образует связь металл - углерод, гидрогенолиз этой связи приводит к конечному продукту и гидриду переходного металла, снова включающемуся в реакцию. [20]
В работе впервые показано, что гидриды хрома-с высоким содержанием водорода проявляют активность в реакции гидрирования бензола до циклогексана. На основании данных по дейтеро-водородному обмену сделан вывод о возможности активации молекулярного водорода через стадию растворения его в кристаллической решетке металла. [21]
Кроме того, казалось целесообразным объединить комплексы переходных металлов, способные к активации молекулярного водорода. Материал по 1ЛА1Н4 выделен в отдельный раздел. [22]
Кроме того, казалось целесообразным объединить комплексы переходный металлов, способные к активации молекулярного водорода. Материал по 1ЛА1Н4 выделен в отдельный раздел. [23]
На рис. 9 изображена зависимость логарифма молекулярной каталитической активности промотора от параметров решетки для наибольших межатомных расстояний. Из этого рисунка видно, что скорость гидрирования коричной кислоты зависит в первую очередь от возможности активации молекулярного водорода. [24]
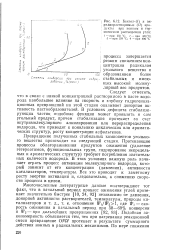 |
Бензол - ( / и пи - ридинрастворимыс ( / / продукты при ионном и термическом растворении угля. [25] |
Превращение полученных стабильных компонентов угольного вещества происходит на следующей стадии. Протекающие процессы облагораживания продуктов ожижения ( удаление гетероатомов, функциональных групп, гидрирование непредельных и ароматических структур) требуют потребления значительных количеств водорода. В этих условиях важную роль начинает играть процесс активации молекулярного водорода, который зависит от его концентрации ( давления), активности катализаторов, температуры. Все это приводит к заметному росту энергии активации и, следовательно, к снижению скорости процесса в целом. [26]
Первый путь предполагает использование низкомолекулярных диффузионно-подвижных переносчиков электрона ( медиаторов), способных акцептировать электроны с электрода и отдавать их активному центру фермента. Этот механизм используется в большом числе ферментативных электродных систем, в частности, в реакциях с участием гидрогеназ - биологических катализаторов активации молекулярного водорода. В системе гидрогеназа - метилвиологен - угольный электрод удается электрохимически окислять водород без перенапряжения в условиях, близких к равновесным. Механизм прямого переноса электронов по пути электрод - активный центр фермента уже реализован в реакции электрохимического восстановления кислорода до воды с участием медьсодержащей оксидазы, в реакции электровосстановления водорода с помощью гидрогеназы. [27]
Возможно, влияние водорода связано со следующим. Технический хлорид алюминия всегда содержит прямеси хлоридов переходных металлов - железа и титана. Представляется вероятным, что именно наличие примесей хлоридов переходных металлов к хлориду алюминия и образование из них в условиях изомеризации комплексных соединений с высоконенасыщенными побочными продуктами изомеризации приводят к активации молекулярного водорода. [28]
Рассмотренный в работе материал иллюстрирует также основное, принципиальное ограничение термодинамического метода предвидения каталитической активности, связанное с тем, что критерий ( 1) не определяет абсолютной каталитической активности. В пределах каждой такой группы выполняется принцип энергетического соответствия и имеется свой оптимальный катализатор, например платина среди переходных металлов и закись-окись кобальта - среди простых окислов. В то же время абсолютная каталитическая активность катализаторов, в одинаковой степени отвечающих критерию оптимума, но принадлежащих к разным группам, отличается на несколько порядков. Это свидетельствует о различиях в элементарном механизме одного и того же каталитического процесса на катализаторах разной природы. В данном случае эти различия связаны, по-видимому, с особенностями активации молекулярного водорода на переходных металлах, непереходных металлах и окислах. [29]
Страницы: 1 2