Активация - фермент
Cтраница 2
Еще более усложняется механизм регуляции транскрипции у эукариотов в связи с активацией фосфорилирующего фермента второй системой матричной регуляции, зависимой от цАМФ, с одной стороны, и стимуляцией метилирующего фермента АМФ, Образующимся из цАМФ при участии цАМФ - фосфодиэстеразы - с другой. Именно среди негистоновых белков и обнаружен этот фермент. [16]
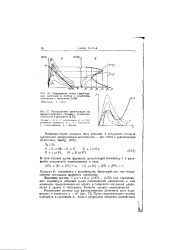 |
Определение числа стационарных состояний в системе с угнетением субстратом и продуктом. [17] |
Продукт Р, связываясь с ингибитором, блокирует его, что тождественно активации фермента продуктом. [18]
 |
Принцип фермент-субстратного контакта.| Фермент-субстратный комплекс ( пептидаза. [19] |
Эта теория дает возможность расширить представления о ферментативном катализе и объяснить механизм ингибирования и активации ферментов. [20]
Наряду с практическими достижениями в сборнике приведены результаты исследований по репарации мутационных повреждений, активации ферментов с помощью супермутагенов, природе стимуляции, индуцированной слабыми дозами мутагенов. [21]
В большинстве исследований по металлактивированным ферментам делались попытки оценить специфичность взаимодействия либо изучением степени активации фермента различными ионами металлов в стандартных условиях, либо в ряде случаев измерением кажущихся констант активации и максимальных скоростей для тех ионов металлов, которые вызывают существенную активацию. [22]
Так, при исследовании аскорбатоксидазы данные о неконкурентном влиянии рН были подкреплены данными о неконкурентной активации фермента ионами галогенов. Эти два ряда данных позволяют уже довольно уверенно утверждать, что между различными формами фермента в данной реакции существует равновесие. [23]
Наиболее очевидным свойством ионов металлов, которое могло бы помочь в объяснении их роли при активации фосфат-переносящих ферментов, является положительный заряд. [24]
Вместе с тем участие марганца в обмене липидов связано с его ролью в синтезе холестерина, объясняемой специфической активацией фермента диметилаллилтрансферазы ( КФ 2.5.1.1), катализирующей синтез фарнезилпирофосфата путем конденсации геранил - и изопентенилпирофосфата. Этот процесс является важным этапом синтеза ланостерниа - предшественника холестерина. Фермент проявляет свою активность только в присутствии металла, причем при низких концентрациях марганец в 40 раз эффективнее магния. [25]
Интенсивное изучение Мейстером [375] механизма реакции глу-таминсинтетазы из мозга овец указывает на то, что ион двухвалентного металла, необходимый для активации фермента, участвует в образовании комплекса фермент - АТФ. Этот вывод основан на изучении различных реакций, катализируемых ферментом, а также того, какие М2 требуются для связывания субстратов и защиты фермента от инактивации. Поэтому для дальнейшего понимания механизма активации под действием М2 необходимы исследования глутаминсинтетазы с использованием методов, которые бы дали информацию об окружении иона металла. [26]
В число биологических функций этих ионов входят поддержание химического потенциала, посылка и передача нервных сигналов; кроме того, путем ком-плексообразования они усиливают такие функции лигандов, как активация ферментов и поддержание структуры тканей. [27]
Мы привели нарочито грубый пример с целью отчетливо показать, что неконкурентное поведение могут вызвать причины, не имеющие отношения к равновесному состоянию системы, даже если имеет место активация фермента или действует модификатор столь малого размера, как гидроний-ион. Именно потому, что на практике можно встретиться с более тонкими конформационными изменениями фермента, сначала нужно попытаться выяснить, не обусловлено ли неконкурентное поведение изменениями физических свойств белка, и лишь в случае отрицательного ответа можно приписать его наличию равновесия. Например, в упомянутом выше случае аскорбатоксидазы при анализе активирующего влияния хлорида были использованы методы седиментации, гель-фильтрации и спект-рофлуориметрии. При этом ни дезагрегации, ни конфор-мационных изменений фермента обнаружено не было, что дало основание допустить возможность приближенного равенства Кт и / G для аскорбата. [28]
Эйген и Гаммес [42] измеряли константы скорости замещения молекул воды металлами при образовании металлсодержащих комплексов, пытаясь при этом выявить какие-либо полезные закономерности, которые можно было бы распространить на случаи активации ферментов металлами. В соответствии с полученными результатами был составлен ряд, отражающий порядок возрастания скорости замещения: СиСа Zn Mn Fe Со Mg Ni. Здесь мы имеем несколько иную последовательность по сравнению с порядком возрастания устойчивости комплексов; следует, однако, отметить, что в одном случае мы имеем кинетические параметры, а в другом - равновесные. [29]
Значительное повышение скорости синтеза дезоксирибону-клеиновой кислоты в печени кроликов, затравленных плутонием, не сопровождалось, однако, повышением концентрации ДНК-Было высказано предположение, что это явление также частично связано - с повышением распада нуклеиновых кислот в результате активации ферментов, в первую очередь ДНК-аз. [30]
Страницы: 1 2 3 4