Активация - электрод
Cтраница 3
Активация электрода происходит, по-видимому, в результате большой пористости оксидной пленки. Ионы, участвующие в электродной реакции, имеют возможность разряжаться как на Fe3O4, так и на железе через поры. Измерения показали, что адсорбция серы является необратимой. Анализируя кривые потенциал-время для вороненых анодов, мы установили, что потенциал вороненых анодов быстро стабилизируется во времени, и его значение остается постоянным. Очевидно, при данной плотности тока происходил процесс разрушения существующего поверхностного окисла. [31]
Активация электродов проводилась по методу, описанному в разд. [32]
Время одиночного электролиза Т0 0 в ячейке с неактивиро-ванным рабочим электродом составляет - 5 мин. Активацией электрода при потенциалах выделения кислорода и водорода, устанавливаемых последовательно, это время может быть уменьшено почти вдвое. [33]
Известно также, что на металлах группы платины после их контакта с органическими соединениями образуются углеродные частицы. В ходе анодно-катодной активации электрода происходит очистка его поверхности от таких частиц. [34]
Для снижения перенапряжения водорода были предложены различные способы так называемой активации электродов путем нанесения на их поверхность электролитически различных металлов ( молибдена, вольфрама, ванадия) или сплавов. Эффект, обусловленный активацией электродов, сохраняется в течение длительного времени только при условии тщательной очистки электролита от примесей солей железа. В этом случае катоды, активированные никелевым покрытием, содержащим серу, обеспечивают снижение напряжения на ячейке на 2 % в течение двух лет. [35]
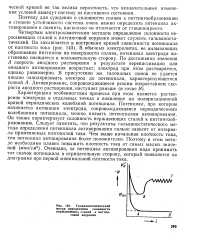 |
Гальваностатический метод определения склонности нержавеющих сталей к питтинговой коррозии. [36] |
Характерными особенностями процесса при этом является растворение электрода в отдельных точках и появление на поляризационной кривой периодических колебаний потенциала. Потенциал, при котором начинается активация электрода, сопровождающаяся периодическими колебаниями потенциала, можно назвать потенциалом активирования. Он также характеризует склонность нержавеющих сталей к питтингообразованию. Следует заметить, что результаты гальваностатического метода определения потенциала активирования сильно зависят от интервала применяемых плотностей тока. Чем выше начальная плотность тока, тем потенциал активирования более положителен. Очевидно, за потенциал активирования надо принимать тот скачок потенциала в отрицательную сторону, который появляется на диаграмме при первой минимальной плотности тока. [37]
Скорость окисления углеводородов на электроде возрастает, если потенциал электрода кратковременно повышать до 0 9 в. Уменьшение тока во времени после активации электрода зависит от природы углеводорода и его парциального давления и вызвано адсорбцией углеводорода на поверхности. [38]
Важнейшей эксплуатационной характеристикой ампульной батареи является время приведения ее в действие. Оно определяется как суммарное время, необходимое для заливки элемента электролитом и активации электродов. Следовательно, время приведения в действие элемента батареи на рис. 36.1 будет равно промежутку от момента подачи импульса тока на электровоспламенитель до момента достижения элементом номинального напряжения, а время активации - от момента появления напряжения до момента достижения им номинального значения. [39]
Тройные системы Ag - А1 - Ni, Ag-Al-Fe, Ag-Zn-Ni и Ag-Zn-Fe являются наиболее интересными, но они еще не изучены. Выбор серебряных сплавов Ренея ограничен тем, что электродный скелет не должен подвергаться коррозии при активации электродов извлечением растворимых компонентов. [40]
Для того чтобы получить данные о кинетике процесса коррозии, мы систематически сочетали измерение кривых поляризации потенциостатическим путем с микрокинематографией. Этот последний метод состоит в кинематографической регистрации микроскопических данных, наблюдаемых во время быстрого развития процесса активации электрода. [41]
При определенном сочетании этих факторов возникает язвенная коррозия. Число дефектных мест на периферии развивающихся язв прогрессивно возрастает, что приводит к генерализации внутренней адсорбции и полной активации электрода. [42]
Поскольку трифторуксусная кислота в комбинации с подходящими электролитами обладает широким анодным окном ( до 2 1 В относительно Ag / Ag и 2 3 В относительно нас.к.э.) [210, 213], в этой системе становится возможным окисление насыщенных углеводородов. Запись кривых плотность тока - потенциал в стационарном состоянии и препаративный ЭКП этих субстратов часто выполняют при импульсной активации электрода. Этот процесс включает короткую периодическую пульсацию потенциала электрода до величины примерно О В, что предотвращает чрезмерное падение тока при рабочем потенциале. На основании электрохимических измерений предполагается, что до лимитирующей стадии и в ней самой происходит перенос одного электрона. [43]
Кривая 1 относится к чистому железу, а кривые 2, 3 4 и 5-к железу которое поглотило, соответственно 0 6 - Ю16, 0 9 - 1016, 2 - Ю15 и 3 3 - 1015 молекул кислорода на 1 см2 истинной поверхности. Из этих данных видно, что при увеличении количества поглощенного кислорода вначале наблюдается смещение анодных кривых и сторону более отрицательного потенциала, что свидетельствует об активации электрода. При дальнейшем увеличении количества поглощенного кислорода кривые анодной поляризации смещаются в сторону более положительных потенциалов, и происходит пассивация железного электрода. Максимальная активация соответствует увеличению скорости анодного процесса в 7 раз. Из полученных данных следует, что максимальное смещение потенциала в отрицательную сторону, вызванное кислородом, соответствует поглощению 1 2 - 1015 молекул па 1 см2 истинной поверхности. [44]
Свыше тысячи композиций электродов было испытано таким образом. Были исследованы состав, распределение частиц по размерам, форма частиц и величина их поверхности, определяемая методом низкотемпературной адсорбции азота для различных комбинаций порошков металлов и сплавов и методики активации электродов катализатором. [45]
Страницы: 1 2 3 4