Активирование - молекула
Cтраница 1
Активирование молекулы введением заместителей I рода в случае пиридина сказывается особенно сильно: 2-амино 15 1в 2-ацетиламино - 17 и 2-окси-производные пиридина меркурируются в водном или спиртовом растворе на холоду. Хинолин 14 18 изохинолин 14 19 метилхинолины18 20 меркурируются также в довольно жестких условиях: при нагревании с уксуснокислой ртутью до 150 в течение нескольких часов. Хинолин дает при этом два мономеркурированиых в 3 и 8 положения продукта и димеркурировапное соединение. Ртуть в изо-хинолине вступает в пиридинное кольцо в - положение к азоту. [1]
Активирование молекулы введением заместителей первого рода в случае пиридина сказывается особенно сильно: 2-амино - [604-605] и 2-оксипроиз-водные пиридина меркурируются в водном или спиртовом растворе на холоду. Ацетиламинопиридин при слабом нагревании с уксуснокислой ртутью в метиловом спирте [605] или с окисью ртути [606] прямо образует симметричное соединение вероятного строения. [2]
Активирование молекулы перекиси водорода, превращение ее из НО ОН в О: ОНЬ происходит в случае пероксидазы за счет энергии, выделяющейся при окислении субстрата, в случае каталазы - за счет энергии, выделяющейся при соединении двух атомов кислорода в молекулу. [3]
Фотооблучение притеняют для активирования молекул веществ и в различных областях физЦко - органической химии органической и неорганической химии фотобиологии и других отраслях. В промышленных условиях фотооблучение применяют в процессах сульфохлорирования, сульфоокисления и других. В результате поглощения квантов энергии УФ-света в полиэдрах твердых катализаторов и молекулах углеводородов и соединений на их основе проходят процессы с перераспределением электронов и другие процессы которые переводят полиэдры в твердом катализаторе и молекулы углеводородов в возбужденное состояние. [4]
В условиях электрического разряда активирование молекул происходит в результате соударения с быстрыми электронами. При этом энергия поступательного движения электрона превращается в энергию возбуждения молекулы. Происходит либо распад молекулы на атомы, радикалы или ионы, либо возбуждение ее, либо образование молекулярного иона. В результате образуется большое число различных активных частиц - атомов, радикалов, ионов, возбужденных молекул, обладающих большим запасом энергии. Высокая реакционная способность этих частиц создает возможности для параллельного протекания многочисленных химических процессов, что приводит к получению сложных смесей разнообразных продуктов. Трудность разделения таких смесей является главным недостатком этого метода. [5]
Иными словами, происходит активирование молекулы СО. [6]
Поэтому, вероятно, активирование молекул водорода затрудняется настолько, что метан не образуется. [7]
Этот фактор является мощным средством активирования молекул. Существуют реакции, которые не удается провести другими путями, кроме фотохимического. Однако в промышленных условиях фотохимические реакции находят пока ограниченное применение. Это объясняется прежде всего недостаточной изученностью реакций фотохимического синтеза органических веществ, а также тем, что из многих фотохимических реакций практический интерес представляют лишь реакции, идущие по цепному механизму. [8]
По-видимому, присутствие нитрогруппы необходимо для активирования молекулы в реакции азосочетания, поскольку диэтиловый эфир гомофталевой кислоты в подобную реакцию не вступает. Однако в случае ангидрида гомофталевой кислоты получают 2-фенилфталазон - 4-карбоновую кислоту [40] ( стр. [9]
Данная группа в составе молекул может способствовать активированию молекулы в этом смысле двумя способами, между которыми, однако, не проводилась отчетливая граница. [10]
Последняя представляет энергию ( на 1 г-мол), необходимую для активирования молекул до состояния, при котором они становятся способными к реакции. [11]
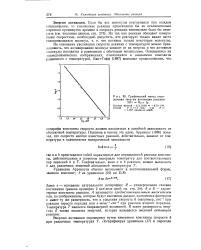 |
Графический метод определения энергии активации реакции 2HI - - Нг 1г. [12] |
На основании увеличения скорости реакции с температурой можно предположить, что активирование молекул зависит от их энергии и что активные молекулы находятся в равновесии с обычными молекулами. [13]
Оно заключается в образовании реакцноннсспособного оародыша, например радикала, при активировании молекулы мономера. Для этого требуется энергия порядка 10 - 25 ккал. Отдельные молекулы могут активироваться под действием света, или при образовании перекиси из олефпна под действием кислорода воздуха и последующем ее расщеплении, или в результате реакций распада нестойких веществ, при которых образуются радикалы, или, наконец, под действием тепла. Это приводит ко второй стадии-стадии роста цепи. [14]
Оно заключается в образовании реакционноспособного зародыша, например радикала, при активировании молекулы мономера. Для этого требуется энергия порядка 10 - 25 ккал / моль. Отдельные молекулы могут активироваться под действием света, или при образовании перекиси из олефина под действием кислорода воздуха и последующем ее расщеплении, или в результате реакций распада нестойких веществ, при которых образуются радикалы, или, наконец, под действием тепла. Это приводит ко второй стадии - стадии роста цепи. [15]
Страницы: 1 2 3 4