Активирование - поверхность
Cтраница 2
Для активирования поверхности железа железные опилки кипятят с кислотой до введения нитробензола, при этом растворяется имеющаяся на ней тонкая пленка окислов. [16]
Возможность активирования поверхности Мк и М определяется прежде всего их составом, характером роста на них окисных пленок в процессе изготовления, хранения, сборки и пайки деталей, а также конструкционными и масштабными факторами изделия и его массой. [17]
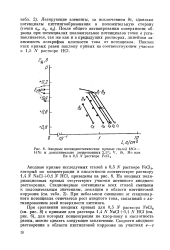 |
Анодные потенциостатические кривые сталей 18Сг. [18] |
После общего активирования поверхности образца при потенциалах положительнее потенциалов точек в устанавливается, так же как и в предыдущих растворах, линейная зависимость логарифма плотности тока от потенциала. [19]
Рассмотренные методы активирования поверхности имеют общий недостаток - опасность латентной коррозии в случае подложек, имеющих макропоры и капиллярные щели, в которых могут сохраняться соляная кислота, хлориды олова и палладия даже после тщательной промывки. Введение в состав подложки или в покровный лак каталитического агента позволяет этого избежать. В органическое связующее, входящее в стеклопластик, вводят ацетат палладия. Его количество должно быть минимальным, чтобы не ухудшить электрические свойства диэлектрика. Стеклопластик с введенным катализатором требует проведения предварительной операции травления поверхности подложки для удаления полимерной сетки и вскрытия катализатора ( см. гл. [20]
Другой причиной активирования поверхности электрода может явиться изменение соотношения скоростей ее пассивирования и обновления при повышении отрицательного потенциала катода. [21]
В ходе активирования па поверхности диэлектрика образуются каталитические центры, являющиеся инициаторами процесса автокаталитического восстановления металла. Наиболее универсальными и удобными являются химические методы активирования в жидкой фазе. Они применимы для любых поверхностей. Суть этих методов заключается в том, что на активируемую поверхность наносят малые количества метал лов - катализаторов ( активаторов) или насыщают поверхностные слои сильными восстановителями, способными в растворе химической металлизации легко восстанавливать ионы осаждаемого металла. [22]
Одновременно с активированием поверхности происходит ее очистка от загрязнений, которые усугубляются на изделиях при обработке электростатическим зарядом. [23]
Среди перечисленных операций активирование поверхности является определяющей в обеспечении сцепления. Недостатком химического травления металлов в различных растворах кислот являются неравномерное растворение дефектного слоя, неизбежное перетравливание поверхности, водородная хрупкость. Электрохимическое травление ( анодная обработка) отличается высокой скоростью и позволяет избежать неравномерного удаления деформированного слоя благодаря пассивированию активных центров. [24]
За сенсибилизацией следует активирование поверхности в 1 % - ном растворе азотнокислого серебра при комнатной температуре в течение 1 - 2 мин. [25]
Как видно, активирование поверхности никеля ( правый снимок на рис. 222) в растворе 20 % - ной серной кислоты в течение 5 - 8 сек. [26]
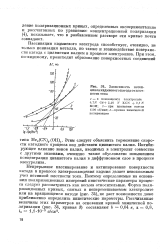 |
Зависимость потенциала кадмиевого катода от плотности тока. [27] |
Непрерывное пассивирование и активирование поверхности катода в процессе электроосаждения кадмия делает невозможным учет истинной плотности тока. Поэтому определяемые на основании поляризационных измерений кинетические параметры процесса следует рассматривать как весьма относительные. Форма поляризационных кривых, снятых в неперемешиваемом электролите или на вращающемся катоде ( рис. 34), не дает возможности даже приближенно определить кинетические параметры. [28]
Широкое применение для активирования поверхности печатных плат нашли так называемые коллоидные, или совмещенные, растворы, получаемые обычно смешиванием солянокислых растворов PdCl2 и SnCb. При этом образуются интенсивно окрашенные растворы координационных соединений анионного типа - PdSnmCl -, которые характерны и для других металлов платиновой группы. Показано, что присутствие коллоидных частиц в таких растворах значительно увеличивает силу активации. Последняя зависит также и от размеров коллоидных частиц. Указывают, что оптимальными являются частицы размером около 2 нм. Последующая акселерация это соотношение увеличивает до 3 или 4, а в растворах металлизации оно достигает 6 и после этого поверхность покрывается осажденным металлом. [29]
Вклад механического фактора активирования поверхности значительно меньший. Эти примеры показывают, что скорость локальной коррозии может достигать значительных величин; сторонники электрохимической гипотезы считают это основой механизма коррозионно-механического разрушения металлов. [30]
Страницы: 1 2 3 4