Активность - платиновый катализатор
Cтраница 2
В отличие от реактора конверсии метана реактор конверсии бензина не имеет в верхней части слоя инертного наполнителя, а заполнен платиновым катализатором, стабилизирующим экзотермическую реакцию неполного окисления даже при высокой скорости реакционного потока ( более 3 тыс. м3 / ч на 1 л 3 поверхности) катализатора. Активность платинового катализатора в присутствии серы не снижается. [16]
Если кислород содержится в очищаемом аргоне в количествах, превышающих стехиометрическое по отношению к горючим примесям на 5 - 10 %, Н2, СО, СН4 могут быть окислены в присутствии катализаторов при более низких температурах и высоких объемных скоростях. При окислении СН4 активность платинового катализатора значительно ниже, чем палладиевого: температура полного окисления СН4 на палладиевом катализаторе 520 - 570 К при объемной скорости до 25 000 ч 1; на платиновом катализаторе полное окисление метана не наблюдается даже при 750 - 800 К. [17]
Содержащиеся в сырье платформинга органические соединения двухвалентной серы оказывают сильное влияние на активность платиновых катализаторов. Влияние природы сераорганических соединений на активность платиновых катализаторов изучено недостаточно; в немногих работах, посвященных этому вопросу, высказываются противоречивые мнения. [18]
Содержащиеся it сырье платформинга органические соединения двухвалентной серы оказывают сильное влияние на активность платиновых катализаторов. Влияние природы сераорганических соединений на активность платиновых катализаторов изучено недостаточно; в немногих работах, посвященных этому вопросу, высказываются противоречивые мнения. [19]
 |
Изменение дисперсности d платины и палладия [ 0 4 % ( масс. ], нанесенных на оксид алюминия, при прокаливании ( 650 С в токе водорода и кислорода. [20] |
Начальные активности нанесенных платинового и палладиевого катализаторов ( с содержанием 0 1 % металла) близки. Прокаливание в течение 70 ч при 900 С на воздухе по-разному сказывается на активности катализаторов; палладиевый катализатор в результате прогревания мало изменяет активность, тогда как активность платинового катализатора значительно снижается. [21]
Пара-орто-превращение при высоких температурах изучалось на металлах в различной форме, на солях и на окислах; опыты затрудняются отравляющим действием кислорода, сероводорода и других типичных катализаторных ядов и смазки для кранов. Наблюдается параллелизм между активностью катализаторов в процессах па-ра-орто-превращения и гидрогенизации; в обоих случаях платина, никель и железо гораздо эффективнее серебра, меди или золота. Для обоих видов реакции небольшие количества кислорода повышают активность платинового катализатора. Кажущийся порядок реакции для процесса превращения лежит во всех случаях между нулем и единицей; это указывает на то, что реакция идет в адсорбированном слое ( Успехи физической химии, гл. [22]
 |
Кривые распределения частиц платины. [23] |
Рост частиц платины наблюдали в процессе работы катализатора ШПК-1 ( содержание Pt в нем - 0 1 %) в токе отработавших газов дизельного двигателя [ 30, с. Наблюдаемое спекание частиц Pt приводит к уменьшению поверхности активной фазы и является, по-видимому, причиной снижения активности платинового катализатора при его продолжительной работе в среде отработавших газов двигателя внутреннего сгорания. [24]
Применение катализаторов значительно понижает температуру сгорания газов, создает более благоприятные условия для их разделения и ускоряет процесс. Наиболее распространенными катализаторами являются платина и палладий. Их применяют в виде проволоки, капилляров или же наносят на носитель. От воздействия следов аммиака активность платинового катализатора со временем падает. Активность платины восстанавливают обработкой ее концентрированной азотной кислотой. [25]
Мэкстед [181] показал, что сероводород не только ослабляет каталитическую активность палладия, но также влияет и на окклюзию водорода. Он количественно исследовал зависимость между способностью к окклюзии и содержанием яда и нашел, что в отношении водорода способность к окклюзии у палладия выражается линейной функцией от содержания серы в катализаторе. Палладий количественно диссоциирует адсорбированный сероводород на серу водород. Зависимость между содержанием серы [181] и активностью платинового катализатора при гидрогенизации олеиновой кислоты линейная до определенной концентрации яда; выше этой величины кривая отравления идет более полого в направлении полной инактивации. [26]
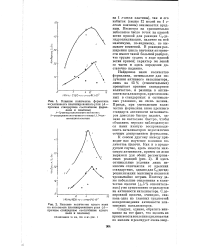 |
Влияние количества формалина на активность платинированного угля ( А - прежнее стандартное соотношение форма.| Влияние количества едкого кали. [27] |
К совсем другому выводу приводит нас изучение влияния количества щелочи. И здесь оптимальные условия лишь немногим отличаются от прежних стандартных, однако для С5 - дегид-роциклизации максимум является чрезвычайно острым. Поэтому даже небольшие отклонения в количестве щелочи ( 5 % относительных) уже существенно отражаются на активности катализатора. С дозировкой щелочи, очевидно, связана одна из главных трудностей воспроизведения активности платиновых катализаторов. [28]
Можно отметить, что каталитические яды, токсичность которых обусловлена наличием в их молекулах кратных связей, как правило, теряют ее, если они в процессе гидрирования превращаются в предельные соединения. Так, при очистке газов для синтеза аммиака, водород которых содержит небольшие количества окиси углерода, перед пуском в главный каталитический реактор газ иногда пропускают через форконтакт, при помощи которого окись углерода превращается в неядовитый метан. Например, Бредиг и его сотрудники [29] при проведении своих, ставших классическими, работ по изучению влияния посторонних веществ на скорость разложения перекиси водорода наблюдали, что активность платинового катализатора, отравленного только окисью углерода, остается низкой до тех пор, пока не пройдет достаточное время для превращения яда в нетоксичную двуокись углерода. [29]
Применяя приведенный выше метод Шеррера, ряд исследователей изучили зависимость между каталитической активностью и размерами частиц катализатора. Виксф и Критенден [482] применили метод Шеррера при изучении влияния активаторов на торможение роста кристаллитов железа в катализаторе, применяемом для синтеза аммиака. Были вычерчены диаграммы восстановленного при температуре около 400 активированного и неактивированного железного катализатора, они показали нормальные резкие линии. Кларк и Аборн [86] исследовали активность платинового катализатора и нашли, что рост активности не следует непрерывно за изменением размера кристаллитов, а проходит через определенный максимум. [30]
Страницы: 1 2 3