Активность - серная кислота
Cтраница 1
Активность серной кислоты очень снижается при ее разбавлении водой, выделяющейся во время реакции, что неизбежно ведет к получению больших количеств отработанной кислоты. Выгоднее работать с 5 - 7 % - ным олеумом, который связывает часть воды, вследствие чего кислота чрезмерно не разбавляется. [1]
Таким образом, активность серной кислоты ( по-собность отдавать протоны) в среде органической кислоты почти в 450 раз выше, чем в водной среде. Растворимость изобутана в рассматриваемых кислотах незначительна: при 13 С составляет сотые доли процента. Во фтористоводородной кислоте растворимость его выше: например, при 26 6 С она равна 2 7 вес. Ббутана пснижается и уменьшается скорость реакции алкилирования. [2]
Добавки различных веществ повышают активность серной кислоты. [3]
Для сопоставления данных пересчитаем коэффициенты активности серной кислоты, приведенные в табл. 9, в моляльную шкалу концентраций. [4]
Хатчинсон и Чандли [945] определяли коэффициент активности серной кислоты в безводной УКСУСНОЙ кислоте, очищенной следующим образом. [5]
Очистка масла при низких температурах ведет к ослаблению активности серной кислоты, но при этом усиливается ее растворяющая способность, в том числе в отношении смол. При низких температурах серная кислота действует как селективный растворитель, удаляющий вредные вещества, растворенные в отработанном масле. [6]
В некоторых случаях, когда нужно ввести несколько суль-фогрупп, активность серной кислоты можно повысить прибавлением фосфорного ангидрида; тот же эффект может быть достигнут повышением температуры реакции. [7]
В тех случаях, когда приходится вводить несколько сульфо-групп, активность серной кислоты можно повысить прибавкой фосфорного ангидрида. [8]
В табл. 10 приведены результаты потенциометриче-ского определения среднего ионного коэффициента активности серной кислоты в моляльной шкале концентраций в несимметричной системе стандартных состояний. [9]
 |
Определение коэффициента активности H2SO4 по. [10] |
Большой интерес представляет сравнение этих данных с результатами независимых определений коэффициента активности серной кислоты каким-либо другим экспериментальным методом, например потенциометрическим. Это интересно еще и потому, что при потенциометриче-ском исследовании серную кислоту рассматривают как электролит. Некоторые результаты потенциометрическо-го исследования растворов серной кислоты в уравнении с данными табл. 9 приводятся в следующем разделе этой главы. [11]
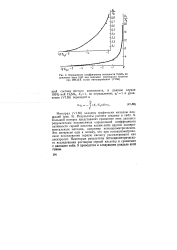
Характер изменения функции кислотности Гаммета ( см. рис. 7) показывает, что активность серной кислоты в значительной степени зависит от содержания в ней воды и резко снижается с увеличением концентрации кислоты. Это особенно заметно в области высоких концентраций. Поскольку функция кислотности серной кислоты в растворе углеводородов намного больше, чем в воде, снижение активности катализатора при ал: илиро-вании будет в первую очередь определяться его разбавлением водой и в меньшей мере растворением в нем высокомолекулярных углеводородов - продуктов побочных реакций. [12]
Активность воды в растворах серной кислоты ( при концентрациях, имеющих место в свинцовом аккумуляторе) изменяется приблизительно в 1 5 раза, в то время как активность серной кислоты в том же интервале концентраций изменяется приблизительно в 20 раз. [13]
Так как степень диссоциации изобутана очень мала, активность серной кислоты при контакте с ним очень велика, и скорость взаимодействия кислоты и углеводорода определяется растворимостью последнего в поверхностном слое кислоты. При низкой концентрации кислоты растворимость изобутана понижается и скорость реакции алкилирования уменьшается. [14]
На рис. 7 показано изменение функции кислотности серной и фтористоводородной кислот в зависимости от их концентрации в воде. Как видно, при равных концентрациях функция кислотности Гаммета и, следовательнэ, активность серной кислоты гораздо выше соответствующих значений для фтористоводородной кислоты. [15]
Страницы: 1 2