Активность - контакт
Cтраница 1
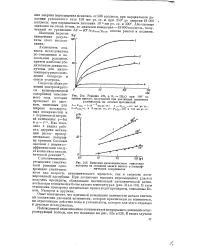 |
Кинетика каталитического окисления водорода на активной закиси никеля в логарифмических координатах. [1] |
Активность контакта исследовалась по отношению к нескольким реакциям, причем наиболее убедительные данные получены для низкотемпературного окисления водорода и окиси углерода. [2]
СО активность контактов, как правило, восстанавливается. [3]
От активности контактов нередко зависит их выбор для конкретных процессов. Для дегидрирования, всегда осуществляемого при высокой температуре, во избежание нежелательных побочных реакций используют менее активные катализаторы - медь, серебро, окислы цинка, хрома, железа и др. Для гидрирования при сравнительно низкой температуре ( 100 - 200 С) чаще всего применяют никель; в более жестких условиях он может вызывать нежелательные реакции, и тогда рекомендуются окисные и хромитные контакты. Тем не менее выбор наиболее подходящего катализатора для каждой реакции является сложной задачей, решаемой в основном экспериментальным путем. [4]
От активности контактов зависит их выбор для конкретных процессов. Для дегидрирования, всегда осуществляемого при высокой температуре, во избежание нежелательных побочных реакций используют менее активные катализаторы - медь, серебро, окислы цинка, хрома, железа и др. Для гидрирования при сравнительно низкой температуре ( 100 - 200 G) чаще всего применяют никель; в более жестких условиях он может вызывать нежелательные реакции, и тогда рекомендуются окисные и хромитные контакты. Тем не менее выбор наиболее подходящего катализатора для каждой реакции является сложной задачей, решаемой в основном экспериментальным путем. [5]
Изучение активности контактов в реакции окисления этилена показало, что удельная активность нанесенного серебра приблизительно равна таковой таблетированного. Отсюда можно сделать вывод, что в кинетическом режиме производительность единицы объема нанесенного контакта определяется величиной поверхности серебра, содержащегося в нем. [6]
Снижение активности контакта во время эксплуатации компенсируется постепенным повышением температуры в реакторах. Однако чрезмерное ее увеличение нежелательно в связи с развитием термических реакций, сопровождаемых повышенным газообразованием и ускоренным закоксовыванием катализатора. [7]
При этом активность контакта 4 и аммиачных контактов отличаются друг от друга. [8]
Для рпределения активности контактов и исследования, кинетики гетерогенных каталитических процессов применяются статический, проточный и наиболее прогрессивный - безградиентный методы. Применение статического метода перемешивающих устройств ( цикл, включающий реактор и циркуляционный насос) позволяет освободиться от таких осложнений. Циклическое устройство с перемешиванием для статического метода было предложено в работах [1, 2], и он был переименован в квазистатический метод. Наиболее часто применяется проточный метод исследования кинетики. Однако в лабораторных условиях ( малые количества контакта) из-за стеночного эффекта, продольного перемешивания, а также неизо-термичности вдоль и по сечению слоя практически - невозможно поддерживать в шихте контакта условия метода идеального вытеснения. [9]
Для регулирования активности контактов мягкого окисления и применения их в удобной форме ( гранулы, шарики определенного размера) используют различные носители; их пропитывают растворами солей, которые затем разлагают; при этом на поверхности носителей образуются окислы металлов. [10]
В процессе катализа активность контакта падает вследствие образования сульфата меди. Поэтому катализатор периодически регенерируют водородом. [11]
Установлено, что активность контакта при температуре 140 и ниже соответствует максимально возможному каталитическому использованию нанесенной фосфорной кислоты. При более высоких температурах наблюдаемая активность контактов ниже рассчитанной, что, невидимому, связано с лимитирующим действием диффузионных процессов. [12]
Поверхностный процесс характеризует активность контакта. В нем можно выделить три стадии: 1) адсорбция одного или большего числа реагирующих веществ, 2) реакция на поверхности, 3) десорбция продуктов реакции. [13]
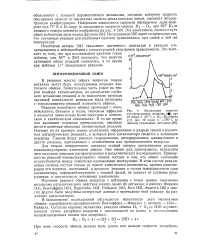 |
Абсолютные скорости о-я-превращения водорода ( при 10 торр и 26 С и Н3 - О2 - обмена ( О при 10 торр и - 196 С на окислах переходных металлов. [14] |
Некоторые авторы [34] связывают активность контактов в реакции о-п-превращения и дейтерообмена с концентрацией электронов проводимости. Это вытекает из того, что при исследовании влияния таких добавок, как А13 к ZnO оказалось, что энергия активации обеих реакций снижалась, в то время как добавки Li прекращали реакцию. [15]
Страницы: 1 2 3 4