Активность - углеводород
Cтраница 1
Активность углеводорода в реакции хлорметилирования зависит как от природы ароматического соединения, так и от наличия и природы заместителей. Присутствие в ароматическом ядре алкильных и алкоксильных групп приводит к ускорению реакции. [1]
Активность углеводородов в условиях полного окисления выглядит следующим образом: трудно окисляются изопентан, толуолj стирол, а изопрен, димеры изопрена, изоамилены, 1 5 9-циклододекатриен, винилциклогексен практически полностью окисляются при температуре 200 С. Труднее всего окисляется изопентан, при температуре 200 С степень его окисления меньше 20 % мае. [2]
Коэффициенты активности углеводородов при бесконечном разбавлении в селективных растворителях, или предельные коэффициенты активности, являются важной термодинамической характеристикой степени неидеальности растворов. Дортмундский банк данных содержит сведения о 12700 чистых веществах и смесях из 32 тысяч литературных источников. [3]
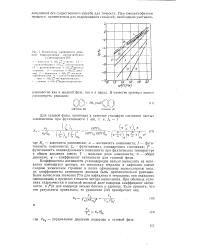 |
Константы равновесия реакций гидрирования ароматических углеводородов. [4] |
Коэффициенты активности углеводородов нельзя вычислить на основании имеющихся данных; но поскольку тетралин и нафталин имеют г. е, мическое роение и почти одинаковые молекулярные веса их коэффициенты активности должны быть приблизительно равными Были вычислены значения / / я для нафталина и тетралина; они оказались одинаковыми в пределах точности метода вычисления. При обычных условиях гидроочистки и высокой мольной доле водорода коэффициент активности и / / я для водорода весьма близки к единице. [5]
Коэффициенты активности углеводородов, имеющих одинаковое число углеродных атомов в молекулах, в полярных растворителях снижаются в ряду: алканалкеналхади-еналкин ароматический углеводород. Это соответствует возрастанию электронодонорной способности углеводородов и стабильности я-комплексов ненасыщенных и ароматических углеводороде с молекулами растворителей - акцепторами электронов. [6]
Предельные коэффициенты активности углеводородов С5 - С8 определяли, как правило, при невысокой температуре, чаще всего при 30 С. [7]
Отметим, что активность углеводородов с третичным углеродным атомом зависит от характера соединения в целом, а не только от наличия группы СН. [8]
В таблицах приведены предельные коэффициенты активности углеводородов в 506 селективных растворителях, последовательность которых определяется их брутто-формулами. [9]
Методом ГЖХ были определены предельные коэффициенты активности углеводородов С6 - Се различных классов в 12 циклических амидах-т-производных пирролидона-2, пиперидона-2, капролактама, сукцинимида при 30 С. [10]
Методом газо-жидкостной хроматографии были определены коэффициенты активности углеводородов различных классов в изомерах крезола, на базе которых рассчитана селективность этих растворителей в различных углеводородных системах. На базе исследований избирательной и растворяющей способности изомеров разработано необходимое соотношение фенола и крезолов, которое при изменении содержания одного из изомеров крезола позволит сохранить неизменным качество деасфалътизата. [11]
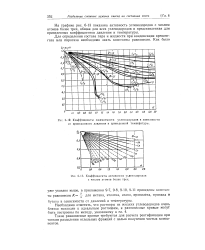 |
Коэффициенты сжимаемости углеводородов в зависимости от приведенного давления и приведенной температуры.| Коэффициенты активности углеводородов с числом атомов более трех. [12] |
На графике рис. 6 - 13 показана активность углеводородов с числом атомов более трех, общая для всех углеводородов и представленная для приведенных коэффициентов давления и температуры. [13]
В справочнике представлены экспериментальные данные о коэффициентах активности углеводородов при бесконечном разбавлении в 506 селективных растворителях, полученные методом газожидкостной хроматографии в лаборатории кафедры технологии нефте - и углехимических производств Санкт-Петербургского государственного технологического института. Приведенные данные могут быть использованы для расчета фазовых равновесий жидкость - пар и жидкость - жидкость, для оценки селективности и растворяющей способности растворителей по отношению к углеводородным системам, для выбора эффективных разделяющих агентов в процессах экстракции, экстрактивной и азеотропной ректификации. [14]
Как следует из представленных данных, коэффициенты активности углеводородов в растворителях уменьшаются в ряду: алканалкеналкадиеналкин - что в основном соответствует возрастанию электронодонорной способности углеводородов и стабильности я-комплексов ненасыщенных углеводородов с молекулами растворителей - акцепторов электронов. [15]
Страницы: 1 2 3