Активность - твердая фаза
Cтраница 2
Поскольку в металлургических агрегатах общее давление газа обычно невелико, постольку фугитивности НгО и Н2 можно заменить их парциальными давлениями, а активности твердых фаз постоянного состава положить равными единице. [16]
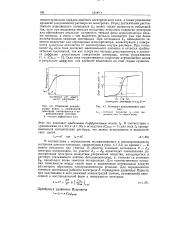 |
Изменение концентрации ионов у поверхности электрода, находящегося в перемешиваемом растворе. 6 - толщина диффузионного слоя.| Катодная вольтамперная кривая. [17] |
Перед достижением рассчитанного равновесного потенциала ЕА может также возникнуть небольшой ток, если при выделении металла вследствие неполного покрытия электрода или образования амальгам активность твердой фазы деполяризатора меньше единицы, в связи с чем выделение металла начинается уже при более положительном значении потенциала. При потенциале ЕА наблюдается заметное выделение или перезарядка деполяризатора, концентрация у поверхности электрода отличается от концентрации внутри раствора. Сила тока ограничивается скоростью передвижения ионов в результате диффузии как наиболее медленного на этой стадии процесса. [18]
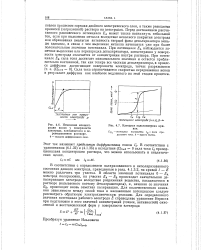 |
Изменение концентрации ионов у поверхности электрода, находящегося в перемешиваемом растворе, б - толщина диффузионного слоя.| Катодная вольтамперная кривая. [19] |
Перед достижением рассчитанного равновесного потенциала ЕА может также возникнуть небольшой ток, если при выделении металла вследствие неполного покрытия электрода или образования амальгам активность твердой фазы деполяризатора меньше единицы, в связи с чем выделение металла начинается уже при более положительном значении потенциала. А наблюдается заметное выделение или перезарядка деполяризатора, концентрация у поверхности электрода отличается от концентрации внутри раствора. Сила тока ограничивается скоростью передвижения ионов в результате диффузии как наиболее медленного на этой стадии процесса. [20]
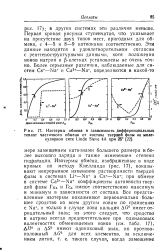 |
Изотермы обмена и зависимость дифференциальных теплот частичного обмена от состава твердой фазы на молекулярном сите Llnde Sieve 4A при 25. [21] |
Изотермы обмена, изображенные в виде кривых по методу Киелланда ( рис. 17), показывают непрерывное изменение растворимости твердой фазы в системах Li - Na и Cs - Na; при обмене в системе Са2 - Na коэффициенты активности твердой фазы Гна и Гса имеют соответственно максимум и минимум в зависимости от состава. [22]
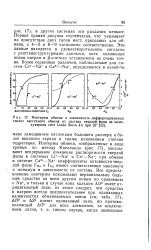 |
Изотермы обмена и зависимость дифференциальных теплот частичного обмена от состава твердой фазы на молекулярном сите Linde Sieve 4A при 25. [23] |
Изотермы обмена, изображенные в виде кривых по методу Киелланда ( рис. 17), показывают непрерывное изменение растворимости твердой фазы в системах Li - Na и Cs - Na; при обмене в системе Са2 - Na коэффициенты активности твердой фазы FNB и Гса имеют соответственно максимум и минимум в зависимости от состава. [24]
Для растворителя практически невозможно достичь предельного тока, при любых значениях потенциала электрода, так как концентрация растворителя неизмеримо большая ( практически постоянна); также не существует предельный ток для твердых веществ, способных к электропревращению, так как активность твердой фазы постоянна. [25]
Оно является для данной системы величиной постоянной и зависит только от температуры ( табл. В. Активность твердой фазы не входит в уравнение ( 2), поскольку активности всех индивидуальных веществ в конденсированном состоянии приняты равными единице. Следует, однако, иметь в виду, что это уравнение верно лишь в присутствии твердой фазы. [26]
Принято считать, что при реакциях в гетерогенных системах, состоящих из твердых и газообразной фаз, изменение количества вещества в твердых фазах не оказывает влияния на состояние равновесия в газообразной фазе. Поэтому активности твердых фаз обычно не входят в выражение для константы равновесия. Естественно, что при высоких давлениях необходимо учитывать рост активности твердых тел по уравнению (1.49), а также адсорбцию и растворение газов в твердых фазах, снижающие активность последних. [27]
Принято считать, что при реакциях в гетерогенных системах, состоящих из твердых и газообразной фаз, изменение количества вещества в твердых фазах не оказывает влияния на состояние равновесия в газообразной фазе. Поэтому активности твердых фаз обычно не входят в выражение для константы равновесия. Естественно, что при высоких давлениях необходимо учитывать рост активности твердых тел по уравнению (1.58), а также адсорбцию и растворение газов в твердых фазах, снижающие активность последних. [28]
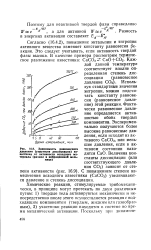 |
Зависимость равновесного давления ( упругости диссоциации известняка от активности исходного материала ( размол в вибрационной мельнице. [29] |
Согласно (16.4.2), повышение энтальпии и энтропии активного вещества изменяет константу равновесия реакции. Это следует учитывать, если активность твердой фазы высока. [30]
Страницы: 1 2 3