Активность - фенол
Cтраница 1
Активность фенолов в реакциях электрофильного замещения настолько велика, что даже формальдегид в кислых растворах реагирует с фенолом. [1]
На активность фенолов и ароматических аминов значительное влияние оказывают заместители в бензольном кольце. Электроно-донорные заместители ( например, алкилы), особенно в орто - и в меньшей степени в мета-положении к группе ОН или - NH2, заметно повышают стабилизирующее действие; электроноакцептор-ные заместители ( например, атомы галоидов) в тех же положениях понижают активность ингибитора. [2]
Коэффициенты активности фенолов на данном сорбенте имеют значения меньше единицы. [3]
Полученные коэффициенты активности фенола в органической фазе учитывают уже все взаимодействия: фенол - фенол, фенол - вода, фенол - растворитель. [4]
За единицу выбрана активность фенола. [5]
В данной работе изучалась активность различных производных пространственно-экранированных фенолов, полифенолов и 3-оксшшридинов, которая оценивалась по их способности тормозить процессы жидкофаз-ного окисления углеводородов и реагировать со свободными радикалами, ведущими цепь окисления. [6]
Имеются некоторые указания о специфической, избирательной активности фенолов относительно тех или других типов микроорганизмов. Однако эти данные недостаточно ясны, чтобы сделать определенные выводы. [7]
Основной катализ сводится к повышению активности фенола в реакции с электрофильными агентами, в данном случае с формальдегидом. [8]
Активность диоксибензолов значительно выше, чем активность фенола; при этом взаимное расположение заместителей имеет здесь, повидимому, такое же значение, которое отмечено в дальнейшем для крезолов: на лягушках и морских свинках минимальные смертельные дозы пирокатехина и гидрохинона равны между собой и составляют около половины минимальной смертельной дозы резорцина. [9]
Как уже говорилось в предыдущем разделе, активность фенола в органических растворителях не прямо пропорциональна его концентрации. Поэтому предварительно необходимо определить анн в тройной системе вода - фенол - растворитель. Для того чтобы эти данные могли быть использованы без большой ошибки для систем, содержащих экстрагаруемый комплекс металла, концентрация последнего в органической фазе должна быть достаточно мала. [10]
При катализе реакции фенола с формальдегидом основаниями повышается активность фенола к электрофильному агенту - формальдегиду. Образующиеся гидроксиметильные производные в щелочной среде ( в отличие от кислой) вполне устойчивы при температуре до 60 С и не подвержены дальнейшим превращениям. Образующиеся в первой реакции диметиленэфирные связи в щелочной среде неустойчивы и разлагаются с выделением формальдегида, превращаясь в метиленовые связи. [11]
Стойкость против деструкции зависит в большей мере также от активности фенола: чем активнее фенол, тем медленнее деструкция. В частности, поликонденсаты на основе резорцина и алкилре-зорцинов деструктируются крайне медленно даже при хранении в горячей воде и свободном доступе воздуха. [12]
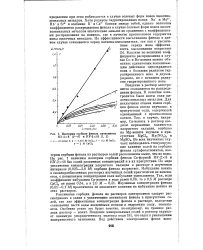 |
Изотермы сорбции фенола катионитом КУ-2Х8 ( 3 - 6 и КУ-2Х16 ( 1, 2. [13] |
Увеличение сорбции фенола из растворов электролитов следует рассматривать в связи с увеличением активности фенола в присутствии солей, так как эффективная концентрация фенола в растворе, вследствие связывания части воды введенными ионами в гидратную воду, повышается. Особенно резко это будет заметно, по-видимому, на границе раздела раствор - ионит. Введение минеральныых солей в раствор нарушает взаимную упорядоченность молекул воды [8], что ведет к уменьшению поверхностного натяжения. [14]
Заместитель, находящийся в пара-положении, не влияет на ориентирующее действие гидроксильной группы и активность фенола в реакциях поликонденсации. Поэтому пара-замещенные фенолы конденсируются с формальдегидом, образуя низкомолекулярные хрупкие и растворимые полимеры. Для получения сетчатых полимеров проводят поликонденсацию смеси пара - амещенных фенолов и незамещенного фенола с формальдегидом. [15]
Страницы: 1 2