Активность - второе - компонент
Cтраница 1
Активность второго компонента В находят обычным путем по формуле (1.17) для всех концентраций сплава. [1]
Вблизи значения XAI вычисление активности второго компонента затруднено, так как подынтегральная функция при этом пределе стремится к бесконечности. Чтобы уменьшить ошибку расчета, желательно иметь данные по активностям компонента А при составах сплава, наиболее близких к чистому веществу А. Следует, конечно, учитывать, что из-за ограниченной точности в определении активности веществ и состава сплава всегда имеется некоторая предельная концентрация, выше которой бессмысленно проводить эксперимент. [2]
Заштрихованная площадь дает логарифм коэффициента активности второго компонента. [3]
Естественно, что на реакционную способность, хлор ангидридов влияет и активность второго компонента - нафтолов. По реак-ционноспособности в реакции ацилирования изученные нафтолы можно расположить в следующий ряд: 2 - нафтол6 - бром-2 - наф - тол 1-нафтол 4-нитро - 1 -нафтол 1-нитро - 2-нафтол 2-нитро - 1И нафтол 2 4-динитро - 1 -нафтол. [4]
Это уравнение позволяет найти коэффициент активности одного компонента бинарного раствора, если известна зависимость коэффициента активности второго компонента от концентрации. Для наиболее удобного использования уравнения Гиббса-Дюгема его следует интегрировать. [5]
Следовательно, если коэффициенты активности одного компонента во всем интервале концентраций больше единицы, то коэффициенты активности второго компонента также должны быть всегда больше единицы. Иными словами, положительным отклонениям от закона Рауля в поведении одного компонента всегда отвечает такое же отклонение от закона Рауля для второго компонента. Несоблюдение этих условий, вытекающих из уравнения ( 184), указывает на ошибочность экспериментальных данных. [6]
В смесях электролитов соль, которая присутствует в более высокой концентрации, определяет характер изменения коэффициента активности второго компонента в тем большей степени, чем сильнее различаются концентрации обоих компонентов. Если коэффициент активности основного компонента при данной ионной силе больше, чем коэффициент активности другого, то последний увеличивается по сравнению с тем значением, которое он имел бы в растворе при такой же ионной силе. Справедливо и обратное положение. [7]
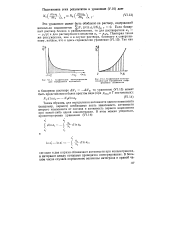 |
Графическое интегрирование для определения активности.| Графическое интегрирование для определения коэффициента активности. [8] |
Таким образом, для определения активности одного компонента ( например, первого) необходимо знать зависимость активности второго компонента от состава и активность первого компонента при какой-либо одной концентрации. [9]
Следовательно, если коэффициенты активности одного компонента во всем интервале концентраций больше единицы, то коэффициенты активности второго компонента также должны быть всегда больше единицы. Цными словами, положительным отклонениям от закона Рауля в поведении одного компонента всегда отвечает такое же отклонение от закона Рауля для второго компонента. Несоблюдение этих условий, вытекающих из уравнения ( 305), указывает на ошибочность экспериментальных данных. [10]
Следовательно, если коэффициенты активности одного компонента во всем интервале концентраций больше единицы, то коэффициенты активности второго компонента также должны быть всегда больше единицы. Иными словами, положительным отклонениям от закона Рауля в поведении одного компонента всегда отвечает такое же отклонение от закона Рауля для второго компонента. Несоблюдение этих условий, вытекающих из уравнения ( 184), указывает на ошибочность экспериментальных данных. [11]
Если коэффициент активности одного компонента больше единицы во всем диапазоне концентраций, то, как следует из уравнения ( 100), коэффициент активности второго компонента также должен быть больше единицы во всем диапазоне концентраций. [12]
Пользуясь ( 48), где сумма аппроксимируется одним членом с максимальным статистическим весом [ этот метод был уже ранее употреблен при переходе от формулы ( 26) к ( 27) ], можно получить выражение коэффициента активности второго компонента. [13]
Следовательно, если коэффициент активности одного компонента непрерывно возрастает с увеличением его концентрации, то такая же закономерность должна иметь место и для второго компонента, а на графике зависимости lg YI / ( - i) и 1е Y2 / ( xi) увеличение коэффициента активности одного компонента должно сопровождаться уменьшением коэффициента активности второго компонента. [14]
Предыдущие рассуждения были основаны на предположении, что в процессе, определяющем скорость диффузии, принимают участие молекулы только одного вещества. Если же в этом процессе участвуют молекулы каждого компонента, то выражение для Д / 7 в уравнении ( 119) должно быть дополнено членом, имеющим отрицательный знак и учитывающим изменение с расстоянием коэфициента активности второго компонента. Однако в виду того, что уравнение ( 142) приводит к результатам, согласующимся с экспериментальными данными, как это будет показано ниже, представляется вероятным, что молекулы только одного из компонентов участвуют в каждом элементарном переходе через активированное состояние при диффузии. Это не следует понимать так, что все скачки совершаются только молекулами одного вещества. В действительности, оба типа молекул могут принимать участие в общем процессе, хотя в каждом элементарном акте, определяющем скорость диффузии, принимают участие только молекулы одного или другого вещества, но не обоих сразу. [15]
Страницы: 1 2